【目的】非共生固氮是农田生态系统中氮素输入的重要途径之一,探明非共生固氮速率、固氮微生物丰度及其群落结构对施肥量的响应,为农业可持续生产提供施肥参考。【方法】试验地点位于东北黑土区,该地块自2012年起一直实行免耕及秸秆还田。田间试验设置6个施氮量处理:0、120、150、180、210、240 kg/hm²,分别记作N0、N120、N150、N180、N210、N240。玉米收获后,采集0-5、5-20 cm土层土壤样品,测定土壤pH和速效氮、磷、钾含量;采用乙炔还原法、定量PCR和高通量测序技术,分析土壤非共生固氮速率、固氮微生物丰度、群落结构多样性。【结果】不同施氮量下,土壤非共生固氮速率为C₂H₄ 0.26~0.63 nmol/(g·d),N150处理0-5和5-20 cm土层土壤非共生固氮速率均最高,分别为C₂H₄ 0.53和0.63 nmol/(g·d);固氮酶基因nifH丰度范围为5.34×10⁶~15.64×10⁶ copies/g,0-5和5-20 cm土层土壤nifH基因丰度的最大值也为N150处理,分别为15.64×10⁶和8.74×10⁶ copies/g。主成分分析(PCoA)结果显示,不同施氮量之间固氮微生物群落结构存在显著差异。各施氮量处理土壤固氮菌群属水平以unclassified_o_Burkholderiales、unclassified_k_norank_d_Bacteria、Skermanella、Methylocystis为优势菌属。Spearman相关性分析结果表明,非共生固氮速率与土壤速效钾含量呈显著正相关,与pH呈负相关;nifH基因拷贝数与土壤速效钾含量呈显著正相关,与施氮量呈负相关。冗余分析显示,nifH群落结构与土壤pH及NH₄⁺-N、NO₃⁻-N、有机碳、全氮、有效磷、速效钾含量呈显著相关。【结论】在长期免耕和秸秆全量还田条件下,施用N 150 kg/hm²有利于增加土壤非共生固氮速率和固氮微生物丰度,丰富群落结构多样性,是该地区较为适宜的施氮量。
关键词:免耕;施肥量;非共生固氮速率;土壤固氮微生物群落;nifH
论文《适宜施氮量提高东北黑土非共生固氮速率和固氮菌丰度》发表在《植物营养与肥料学报》,版权归《植物营养与肥料学报》所有。本文来自网络平台,仅供参考。
一、引言
氮(N)是植物需求量最大的元素,也是限制产量形成的最重要的营养元素。人们普遍追求作物高产,而土壤氮库通常不能满足植物对氮的需求。氮肥的过量使用,导致土壤自身供氮能力下降,破坏了农田生态系统的稳定性,严重影响了我国农业的可持续发展,加剧了生态环境的恶化。
生物固氮过程催化大气中的氮气还原为植物可利用的氮,每年可为农田生态系统提供40~70 Tg N输入,是农业生态系统中重要氮来源之一。生物固氮主要包括两种类型:一是共生固氮,主要由与植物寄主共生的固氮微生物介导;二是非共生固氮,主要由异养、自养菌或某些固氮古菌介导。与共生固氮相比,非共生固氮速率低,但在时间和空间上分布广泛,非共生固氮量约为每年N 0~60 kg/hm²,被认为是土壤生态系统中重要氮输入源。因此,非共生固氮作为一种环境友好、可持续的供氮方式,可以替代部分无机氮肥,为农业生产中过量施氮造成的能源消耗和生态环境污染问题提供替代方案。
nifH基因是固氮菌中编码铁蛋白的基因,具有高度保守性,作为分子标记基因用于研究土壤固氮微生物多样性和群落组成。大量研究表明,土壤固氮微生物的丰度、多样性以及活性受施肥管理和种植方式等多种因素的综合影响。长期定位施肥试验研究发现,高量施用无机肥料(NPK)可能降低固氮微生物群落的丰度,改变固氮群落结构并抑制潜在的固氮能力。肥料对土壤固氮菌群的影响主要体现在通过提供可利用营养物,如有机碳、磷、可利用氮,以及碳氮比的变化,直接影响固氮细菌,也可通过改变土壤性质间接影响固氮细菌。
结合宏基因组技术的研究表明,施用高量氮肥抑制了土壤非共生固氮效率,这可能是当土壤环境中存在较高水平的矿化态氮(NH₄⁺或者NO₃⁻)后,许多固氮微生物会自动关掉固氮功能。非共生固氮为农田生态系统氮素输入的重要途径,土壤有效态氮含量与固氮微生物nifH基因丰度及非共生固氮潜力密切相关。因此,了解不同施氮量下土壤固氮微生物群落及固氮速率的变化,能够有效利用非共生固氮作用,最大程度上优化肥料施用量。
非共生固氮在黑土中的研究此前鲜有报道,关于秸秆还田保护性耕作下不同施氮量对土壤非共生固氮的影响也没有开展系统研究。因此,本研究基于黑土保护性耕作长期定位试验,采用乙炔还原法(测定非共生固氮速率)和高通量测序等技术,分析不同施氮量下土壤理化性质、非共生固氮速率、固氮微生物丰度、固氮菌群落多样性和结构的变化规律,有助于更好地了解黑土长期施肥的生态效应,明晰固氮细菌在农业生态系统中的生态功能,从而促进生物固氮、降低无机氮肥的使用。
二、材料与方法
(一)研究区概况
本试验依托于吉林省长春市中国科学院东北地理与农业生态研究所长春综合试验站(44°00′N, 125°24′E)的保护性耕作长期定位试验。试验区土壤类型为中层典型黑土,壤质粘土。试验区气候属于中温带大陆性季风气候,年平均气温6.4℃,年均降水量为550 mm,降雨量主要集中在6、7、8月。定位试验始于2012年。本研究的微区试验选择秸秆覆盖全量还田的玉米连作免耕小区。除播种外,全年不扰动土壤,前茬秸秆覆盖地表还田。采用联合作业牵引式免耕播种机播种。
(二)微区试验设计
微区试验开始于2021年5月,设置不同施氮量。本试验采用100%秸秆还田(秸秆还田量为11000 kg/hm²),试验中所用氮肥为尿素。为减少扰动,提前将18个高0.3 m、边长0.5 m的正方形PVC框埋入试验小区,并在上面罩一层纱网,避免秸秆被风吹走。
根据东北地区农民习惯施氮量(240 kg/hm²)及优化施氮量(150 kg/hm²),试验设置6个施氮量处理:0、120、150、180、210、240 kg/hm²,分别记作N0、N120、N150、N180、N210、N240。每个处理3次重复,总计18个微区,随机区组排列。5月16日同时进行播种与添加氮肥,各处理P₂O₅和K₂O用量均为78 kg/hm²。每个微区播种两株玉米,播种深度为3~5 cm,化肥施用量根据微区面积分成两份,分别于两株玉米侧下方6~9 cm处深施,与种子相隔3~5 cm。
(三)土壤样品的采集
于2021年7月末,采集0-5、5-20 cm土层土壤样品,每个小区呈“S”形取样,7个采样点,将同一深度的7个样品混合成1个样品带回实验室,测定含水量等基本数据。一部分土壤样品在−80℃冰箱储存,用于测定土壤固氮微生物;一部分土壤样品在4℃冰箱保存,测定非共生固氮速率;另一部分土壤样品自然风干后,用于测定土壤理化性质。
(四)测定方法
1. 土壤理化性质:土壤全量碳氮采用元素分析仪(Flash EA1112, Thermo Finnigan, Italy)测定;土壤微生物量氮(MBN)采用氯仿熏蒸提取,用TOC V_CPU自动分析仪测定(日本岛津)滤液氮含量;土壤无机氮采用全自动连续流动分析仪(SKALAR SAN++, 荷兰)测定;有效磷采用连续流动分析仪(荷兰SAN++ SKALAR)测定;速效钾采用GBC-906原子吸收光谱仪(澳大利亚AAS)测定。
2. 非共生固氮速率测定方法:土壤非共生固氮速率采用乙炔还原法(ARA)测定。将10 g新鲜土壤样品置于密闭性良好的血清小瓶中,置于28℃~30℃培养箱中培养48 h,在无菌条件下将血清小瓶盖换成橡胶塞,用无菌注射器抽出10%的气体,每瓶注入1 mL C₂H₂,再置于28℃~30℃下培养24~48 h。48 h内用气相色谱仪测定待测气体中C₂H₄生成量,具体做法是用无菌注射器从瓶中抽取0.2 mL混合气体注入气相色谱仪(GC)进样柱,测定C₂H₄含量,然后再换算成固氮速率。
分析步骤如下:当高纯He载气以及空气和氢气的流量达到设定值时,打开GC开关,调用GC已设定好的方法,当柱箱温度、检测器温度和进样口温度分别达到60℃、250℃和250℃时,开始点火;于Agilent色谱在线工作站设置好实验参数,待基线趋于稳定后进行样品检测;用进样针抽取顶空气体样品1 mL,进样;待气体样品分组检出后,依据本研究的保留时间(4.7 min)找出乙烯组峰,可得出乙烯组的峰面积数值,通过外标法可校正得出相对应的气体样品乙烯浓度(含量)。乙烯产生量与固氮量最常用的摩尔比值是3∶1,即按C₂H₄:N₂=3:1比例计算。
3. DNA提取和PCR扩增:使用E.Z.N.A.® soil DNA kit试剂盒(Omega Bio-tek, Norcross, GA, U.S.)提取土壤总DNA,随后使用1%琼脂糖凝胶电泳检验DNA提取质量,用NanoDrop 2000微量分光光度计(Thermo Scientific, USA)检测其浓度和纯度,−20℃保存备用。将提取的DNA原液稀释至约10 ng/μL作为PCR扩增模板。扩增引物为带有16 bp头部序列的nifH F(5′−AAAGGYGGWATCGGYAARTCCACCAC−3′)和nifH R(5′−TTGTTSGCSGCRTACATSGCCATCAT−3′)。
扩增程序:95℃预变性3 min后,95℃变性30 s,62℃退火30 s,72℃延伸60 s,用1%的琼脂糖凝胶电泳检测。利用AxyPrep DNA Gel Extraction Kit(Axygen Biosciences, Union City, CA, USA)进行产物回收纯化。利用Illumina公司的Miseq PE300/NovaSeq PE250平台进行测序(上海美吉生物医药科技有限公司)。
4. 实时定量PCR:qPCR采用ABI 7900实时定量PCR系统进行检测,选用的荧光试剂是SYBR Premix Ex Taq TMⅡ。扩增引物是plo F(TGCGAYCCSAARGCBGACTC)和pol R(ATSGCCATCATYTCRCCGGA),扩增体系为15 μL,包含7.5 μL 2×SYBR Premix Ex Taq II,0.3 μL 50×ROX Reference Dye,10 μmol/L的前后引物各0.6 μL,2 μL DNA模板和4.0 μL ddH₂O,每个样品3次重复。扩增程序为95℃预变性30 s,95℃解链5 s,62℃退火30 s,72℃延伸60 s,83℃采集信号10 s,40个循环。梯度稀释标准质粒同时进行荧光定量PCR扩增,计算nifH基因的丰度。
(五)数据分析
生物信息学分析等由上海美吉生物医药科技有限公司完成,原始数据下机后,首先进行数据质控,通过序列拼接、过滤和去嵌合体后得到优化序列,使用UPARSE软件(http://drive5.com/uparse/, version 7.1),根据97%的相似度对序列进行OTU聚类并剔除嵌合体。比对Silva 16S rRNA数据库(v138),设置比对阈值为70%。
基于Chao 1指数和Simpson指数描述固氮菌群落的α多样性。不同处理的Chao 1指数和Simpson指数差异采用One-way ANOVA方法分析,用SPSS软件(version 24.0, IBM, USA)完成统计。土壤固氮菌的群落结构用unweighted-unifrac的PCoA分析,nifH基因的拷贝数、多样性与土壤理化性质的相关性采用Pearson分析。采用Excel 2016对试验数据进行整理。利用SPSS软件对数据进行统计分析。
三、结果与分析
(一)不同施氮量下土壤非共生固氮速率和nifH基因丰度
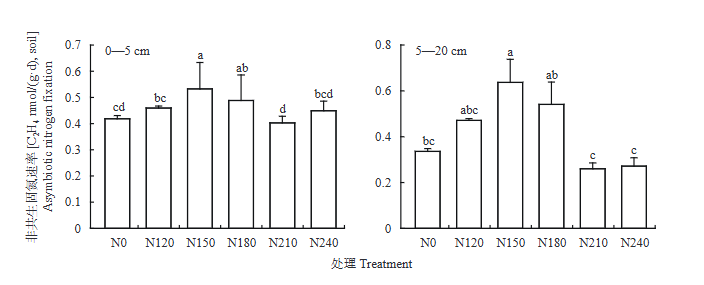
从不同施氮量处理下非共生固氮速率可以看出,随施氮量的增加,0-5和5-20 cm土层土壤非共生固氮速率先增加,在N150处理达到最大,之后降低,在N210处理下最低。0-5 cm土层,N150处理的非共生固氮速率除与N180处理差异不显著外,与其他处理差异均显著(P<0.05);5-20 cm土层,N150处理与N120、N180处理无显著差异,与其他处理差异显著。不同施氮量处理下,土壤的非共生固氮速率为C₂H₄ 0.26~0.63 nmol/(g·d),N150处理0-5和5-20 cm土层非共生固氮速率分别为0.53和0.63 nmol/(g·d)。
0-5 cm土层土壤固氮基因丰度范围是5.34×10⁶~15.64×10⁶ copies/g,随着施氮量的增加,固氮基因丰度呈上升趋势,在N150处理达到最大值,N150处理的固氮基因除了与N120处理差异不显著外,与其他处理均差异显著(P<0.05)。在5-20 cm土层,随着施肥量的增加,固氮基因丰度呈先下降再上升再下降趋势,在N150处理达到最大值,为8.74×10⁶ copies/g,而后随着施肥量的增加而降低,N150处理的固氮基因丰度与N0、N180、N210处理差异不显著,与其他处理差异显著(P<0.05)。
(二)不同施氮量下固氮微生物群落多样性及群落组成
0-5和5-20 cm土层的土壤固氮微生物Shannon指数各处理间差异均不显著。不同施氮量下土壤固氮微生物丰富度(Chao)指数差异显著,在N150处理达到最大值,之后随着施氮量的增加先降低再升高。N150处理与N210处理0-5 cm土层土壤固氮微生物Chao指数差异不显著,与其他处理差异显著。N150处理5-20 cm土层土壤固氮微生物Chao指数与N0、N240处理差异不显著,与其他处理差异显著。
采用加权(weighted-unifrac)算法对不同施氮量下固氮微生物群落结构进行主成分分析,第一主成分和第二主成分分别解释了总体变化的26.39%和12.88%,两者总解释率为39.27%。Adonis(R=0.0428,P<0.05)分析表明,不同施氮量处理间固氮微生物群落结构存在显著差异。
从不同施氮量下固氮菌群属水平的相对丰度来看,0-5 cm土层,unclassified_o_Burkholderiales、unclassified_k_norank_d_Bacteria、斯克尔曼氏菌(Skermanella)为优势菌属,N150处理Skermanella的丰度最大。5-20 cm土层,以unclassified_o_Burkholderiales、unclassified_k_norank_d_Bacteria、甲基孢囊菌属(Methylocystis)为优势菌属,N150处理unclassified_o_Burkholderiales和unclassified_k_norank_d_Bacteria的丰度最大。
(三)相关性分析
从不同施氮量下土壤环境因子与固氮微生物群落相关指标的Spearman相关性分析结果可知,非共生固氮速率与pH呈显著负相关(r=-0.511,P<0.05),与速效钾呈显著正相关(r=0.522,P<0.05)。nifH基因拷贝数与施氮量呈显著负相关(r=-0.519,P<0.05),与速效钾呈显著正相关(r=0.604,P<0.05)。
为了进一步探究不同施氮量下影响nifH基因群落结构的环境因子,进行了冗余分析(redundancy analysis, RDA)。RDA1的变异解释率为22.98%,RDA2的变异解释率为4.79%,总变异解释率为27.77%。nifH群落结构与土壤pH、NH₄⁺-N、NO₃⁻-N、有机碳、全氮、有效磷、速效钾呈显著相关(P<0.05)。
四、讨论
(一)不同施氮量对土壤非共生固氮速率和nifH基因丰度的影响
本研究结果显示,不同施氮量下,非共生固氮速率及nifH基因丰度的最大值出现在N150处理,并不随着施氮量的增加持续增大。有研究也指出,高氮输入会降低生态系统对非共生固氮菌的依赖性,抑制固氮效果。增加氮肥用量会降低非共生固氮速率和nifH基因拷贝数;施用氮肥不仅降低了根际土壤固氮菌占总细菌的比例,也显著降低了固氮酶的活性;也有研究表明,向土壤持续输入氮肥40年后,固氮速率下降50%,固氮菌群落的优势类群相对丰度发生了显著变化。这均和本研究结果一致。
当外源氮进入土壤时,微生物可以提高纤维素水解酶(如β-1,4-葡萄糖苷酶和纤维素二糖水解酶等)的活性,导致纤维素、半纤维素等可被利用的碳源物质越来越少,有效碳源的减少不仅使固氮微生物的生理代谢受到影响,还会阻碍其生物固氮的过程。长期的氮素输入,提高了土壤的氮素含量和生物总量,增加了微生物之间的竞争,此时继续通过耗能方式进行固氮将不利于固氮菌的生存,固氮菌的数量也会逐渐减少。长期施用氮肥增加了土壤固氮基因扩增的难度,从而抑制固氮基因的表达。此外,有些固氮菌对高氮环境的耐受性较弱,长期的氮输入可能不利于这些固氮菌的生存,从而降低了固氮菌的群落丰度。结合本研究团队在东北黑土区典型县域多年的生产实践和田间调查也发现,150 kg/hm²在发挥肥效与促进作物生产协同方面效果最佳,可以作为最适参考施氮量。
(二)不同施氮量对土壤固氮微生物群落多样性及群落结构的影响
农田生态系统中,土壤固氮微生物参与土壤氮循环利用,其群落结构的多样性对农田土壤氮素的固持和循环利用具有重要意义。本研究表明,不同施氮量改变了土壤固氮微生物多样性及群落结构。原因主要有两方面:一是,长期施肥对土壤理化性状(如土壤pH、养分有效性、碳的质量及储量等)的改变以及植物生长,都会直接或间接重塑土壤微生物群落组成和结构;二是,农田长期施用氮肥会降低土壤固氮微生物的竞争力,从而导致其群落结构、组成和多样性的改变。
施肥对固氮微生物多样性和结构有显著的影响,但是影响效果目前还没有得到完全一致的结论。Martensson等研究发现,施用氮磷钾肥对固氮微生物的影响较小。也有研究指出,施肥对表达nifH基因的微生物影响甚微,不同施肥量下施肥土壤nifH的mRNA数量和DNA拷贝数并未发生明显变化。不同研究获得了不一致结论的原因,可能是由于施肥后引起了土壤碳、pH、可利用氮等的改变,其他因素如作物、土壤湿度、土地利用方式和土壤类型等不同,也会导致肥料对固氮菌群落影响效果不同。
(三)东北黑土固氮菌群落结构受多个土壤性质指标共同影响和调控
微生物群落结构的形成是一个复杂的过程,需要多个土壤变量的协同作用。高氮输入的有效性直接影响微生物群落结构。本研究中,非共生固氮速率与速效钾(AK)呈显著正相关,与pH呈负相关。nifH基因拷贝数与AK呈显著正相关,与施氮量呈负相关。nifH基因群落结构受土壤pH、NH₄⁺-N、NO₃⁻-N、土壤有机碳、全氮(TN)、有效磷(AP)、AK的影响显著。
众多研究表明,固氮微生物群落结构对不同施肥量反应敏感,这可能是由于不同施肥模式下土壤理化性质发生改变引起的。在其他研究中也观察到,与氮有关的土壤特性(包括NH₄⁺-N、NO₃⁻-N和TN)是影响土壤固氮群落结构的最主要因素。此外,土壤AP和AK是另外两个重要因素。因此,土壤养分有效性(取决于肥料提供的元素)对固氮群落结构的形成至关重要。何冬华等也研究表明,不同施肥量下土壤理化性质对固氮菌群落的影响较为显著,进一步说明东北黑土固氮菌群落结构由多个土壤性质指标共同影响和调控。不同施氮量导致土壤理化性质的变化是土壤微生物群落变化的主要原因。因此,农田生态系统不同的氮肥用量改变了土壤的理化性质,从而影响土壤固氮速率、nifH基因丰度及群落结构。
五、结论
非共生固氮速率及nifH基因丰度的最大值出现在N150处理,且并未随着施氮量的增加持续增大,说明高氮输入会降低生态系统对非共生固氮菌的依赖性,抑制固氮效果。不同施氮量处理改变了土壤理化性质、固氮微生物多样性及群落结构。非共生固氮速率与速效钾含量呈显著正相关,与pH呈负相关。nifH基因拷贝数与速效钾含量呈显著正相关,与施氮量呈负相关。不同施氮量引起的土壤pH、NH₄⁺-N、NO₃⁻-N、有机碳、全氮、有效磷、速效钾的变化,是调控固氮微生物群落结构变化的主要因子。由此可见,免耕耕作方式下,150 kg/hm²是增加土壤非共生固氮速率和固氮微生物丰度的适宜施肥量。
参考文献
[1] Yuan L, Liu Y, He H B, et al. Effects of long-term no-tillage and maize straw mulching on gross nitrogen transformations in Mollisols of Northeast China[J]. Geoderma, 2022, 428: 116194.
[2] Xu X R, Pei J B, Xu Y D, Wang J K. Soil organic carbon depletion in global Mollisols regions and restoration by management practices: A review[J]. Journal of Soils and Sediments, 2020, 20(3): 1173−1181.
[3] Yu Z H, Hu X J, Wei D, et al. Long-term inorganic fertilizer use influences bacterial communities in Mollisols of Northeast China based on high-throughput sequencing and network analyses[J]. Archives of Agronomy and Soil Science, 2019: 1331−1340.
[4] 巨晓棠. 氮肥有效率的概念及意义: 兼论对传统氮肥利用率的理解误区[J]. 土壤学报, 2014, 51(5): 921−933.
[5] Struckman L. Technological and institutional lock-in and excessive synthetic nitrogen fertilizer use on North American grain and oilseed farms[J]. Nordia Geographical Publications, 2021, 49(5): 93−101.
[6] Davies-Barnard T, Friedlingstein P. The global distribution of biological nitrogen fixation in terrestrial natural ecosystems[J]. Global Biogeochemical Cycles, 2020, 34(3): e2019GB006387.
[7] Ladha J K, Peoples M B, Reddy P M, et al. Biological nitrogen fixation and prospects for ecological intensification in cereal-based cropping systems[J]. Field Crops Research, 2022, 283: 108541.
[8] Kuypers M M M, Marchant H K, Kartal B. The microbial nitrogen-cycling network[J]. Nature Reviews Microbiology, 2018, 16(5): 263−276.
[9] Addo M A, Dos Santos P C. Distribution of nitrogen-fixation genes in prokaryotes containing alternative nitrogenases[J]. Chembiochem, 2020, 21(12): 1749−1759.
[10] Yu L L, Tang Y L, Wang Z G, et al. Nitrogen-cycling genes and rhizosphere microbial community with reduced nitrogen application in maize/soybean strip intercropping[J]. Nutrient Cycling in Agroecosystems, 2019, 113: 35−49.
[11] 邱文静, 栾璐, 郑洁, 等. 秸秆还田方式对根际固氮菌群落及花生产量的影响[J]. 植物营养与肥料学报, 2021, 27(12): 2063−2072.
[12] Zhang J, Zheng M H, Zhang Y J, et al. Soil phosphorus availability affects diazotroph communities during vegetation succession in lowland subtropical forests[J]. Applied Soil Ecology, 2021, 166: 104009.
[13] Fan K K, Delgado-Baquerizo M, Guo X, et al. Suppressed N fixation and diazotrophs after four decades of fertilization[J]. Microbiome, 2019, 7(1): 143.
[14] Wang C, Zheng M M, Song W F, et al. Impact of 25 years of inorganic fertilization on diazotrophic abundance and community structure in an acidic soil in southern China[J]. Soil Biology & Biochemistry, 2017, 113: 240−249.
[15] Lin Y X, Ye G P, Liu D Y, et al. Long-term application of lime or pig manure rather than plant residues suppressed diazotroph abundance and diversity and altered community structure in an acidic Ultisol[J]. Soil Biology and Biochemistry, 2018, 123: 218−228.
[16] Tang Y F, Zhang M M, Chen A L, et al. Impact of fertilization regimes on diazotroph community compositions and N₂-fixation activity in paddy soil[J]. Agriculture, Ecosystems & Environment, 2017, 247: 1–8.
[17] Yeoh Y K, Paungfoo-Lonhienne C, Dennis P G, et al. The core root microbiome of sugarcanes cultivated under varying nitrogen fertilizer application[J]. Environmental Microbiology, 2015, 18(5): 1338−1351.
[18] Van Langenhove L, Depaepe T, Verryckt L T, et al. Comparable canopy and soil free-living nitrogen fixation rates in a lowland tropical forest[J]. Science of the Total Environment, 2021, 754: 142202.
[19] Matson A L, Corre M D, Burneo J I, Veldkamp E. Free-living nitrogen fixation responds to elevated nutrient inputs in tropical montane forest floor and canopy soils of southern Ecuador[J]. Biogeochemistry, 2015, 122(2/3): 281−294.
[20] Xiao D, Xiao L M, Che R X, et al. Phosphorus but not nitrogen addition significantly changes diazotroph diversity and community composition in typical Karst grassland soil[J]. Agriculture, Ecosystems & Environment, 2020, 301: 106987.
[21] Zhang L, Wang X T, Wang J, et al. Alpine meadow degradation depresses soil nitrogen fixation by regulating plant functional groups and diazotrophic community composition[J]. Plant and Soil, 2022, 473(1): 319−335.
[22] Yang Q S, Dong J D, Ahmad M, et al. Analysis of nifH DNA and RNA reveals a disproportionate contribution to nitrogenase activities by rare plankton-associated diazotrophs[J]. BMC Microbiology, 2019, 19(1): 188−208.
[23] Crews T E, Farrington H, Vitousek P M. Changes in asymbiotic, heterotrophic nitrogen fixation on leaf litter of Metrosideros polymorpha with long-term ecosystem development in Hawaii[J]. Ecosystems, 2000, 3(4): 386−395.
[24] Zhang L Y, Zhang M L, Huang S Y, et al. A highly conserved core bacterial microbiota with nitrogen-fixation capacity inhabits the xylem sap in maize plants[J]. Nature Communications, 2022, 13(1): 3361.
[25] Li D J, Wang Z C, Sun X B, et al. Tree species effects on asymbiotic N₂ fixation in subtropical karst and nonkarst forests[J]. Soil Biology and Biochemistry, 2018, 117: 185−190.
[26] Compton J E, Watrud L S, Porteous L A, DeGrood S. Response of soil microbial biomass and community composition to chronic nitrogen additions at Harvard forest[J]. Forest Ecology and Management, 2004, 196(1): 143−158.
[27] Van Deynze A, Zamora P, Delaux P, et al. Nitrogen fixation in a landrace of maize is supported by a mucilage-associated diazotrophic microbiota[J]. PLoS Biology, 2018, 16(8): e2006352.
[28] Li C H, Yan K, Tang L S, et al. Change in deep soil microbial communities due to long-term fertilization[J]. Soil Biology and Biochemistry, 2014, 75: 264−272.
[29] Geisseler D, Scow K M. Long-term effects of mineral fertilizers on soil microorganisms: A review[J]. Soil Biology and Biochemistry, 2014, 75: 54−63.
[30] Levy-Booth D J, Prescott C E, Grayston S J. Microbial functional genes involved in nitrogen fixation, nitrification and denitrification in forest ecosystems[J]. Soil Biology and Biochemistry, 2014, 75: 11−25.
[31] Han L L, Qing W, Shen J B, et al. Multiple factors drive the abundance and diversity of diazotrophic community in typical farmland soils of China[J]. FEMS Microbiology Ecology, 2019, 95(8): 113.
[32] Dai X L, Song D L, Guo Q K, et al. Predicting the influence of fertilization regimes on potential N fixation through their effect on free-living diazotrophic community structure in double rice cropping systems[J]. Soil Biology and Biochemistry, 2021, 156: 108220.
[33] Wang J C, Zhang D, Zhang L, et al. Temporal variation of diazotrophic community abundance and structure in surface and subsoil under four fertilization regimes during a wheat growing season[J]. Agriculture, Ecosystems & Environment, 2016, 216: 116–124.
[34] Martensson L, Díez B, Wartiainen I, et al. Diazotrophic diversity, nifH gene expression and nitrogenase activity in a rice paddy field in Fujian, China[J]. Plant and Soil, 2009, 325: 207−218.
[35] Sun R B, Guo X S, Wang D Z, Chu H Y. Effects of long-term application of chemical and organic fertilizers on the abundance of microbial communities involved in the nitrogen cycle[J]. Applied Soil Ecology, 2015, 95: 171−178.
[36] Liao H K, Li Y Y, Yao H Y. Fertilization with inorganic and organic nutrients changes diazotroph community composition and N-fixation rates[J]. Journal of Soils and Sediments, 2017, 18(3): 1076−1086.
[37] 何冬华, 沈秋兰, 徐秋芳, 等. 不同年限毛竹林土壤固氮菌群落结构和丰度的演变[J]. 土壤学报, 2015, 52(4): 934−942.




