甘蔗(Saccharum spp.)是重要经济作物,提供我国约90%的糖料和40%的生物乙醇。由于其基因组庞大、遗传背景复杂,传统育种很难实现对甘蔗高效的遗传改良。基因组编辑技术是当前生命科学领域的颠覆性技术,可实现对目的基因的精准高效修饰。基因组编辑从早期的锌指核酸酶(zinc-finger nucleases, ZFNs)、类转录因子效应物核酸酶(transcription activator-like effector nucleases, TALENs),到具有里程碑意义的成簇规律间隔短回文重复序列及相关蛋白(clustered regularly interspaced short palindromic repeats/CRISPR-associated protein, CRISPR/Cas)系统,以及CRISPR/Cas系统衍生的碱基编辑和引导编辑,大大推动了植物遗传改良的发展和生物育种的升级。随着甘蔗基因组的破译,基因组编辑技术为多倍体甘蔗的遗传改良提供了全新的技术手段。本文从植物基因组编辑技术的发展、CRISPR/Cas技术的迭代优化、甘蔗遗传转化的发展、甘蔗基因组学的进展及基因组编辑在甘蔗中的应用等方面进行综述,重点探讨了基因组编辑在甘蔗抗倒伏育种中的应用前景,为推动基因组编辑在甘蔗育种中的应用提供了参考。
关键词:植物基因组编辑;CRISPR/Cas系统;甘蔗;抗倒伏育种
论文《甘蔗基因组编辑与抗倒伏研究进展》发表在《生物工程学报》,版权归《生物工程学报》所有。本文来自网络平台,仅供参考。
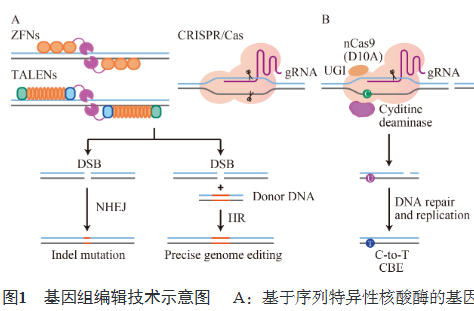
基因组编辑技术从早期的锌指核酸酶(zinc-finger nucleases, ZFNs)、类转录因子效应物核酸酶(transcription activator-like effector nucleases, TALENs),到具有里程碑意义的成簇规律间隔短回文重复序列及相关蛋白(clustered regularly interspaced short palindromic repeats/CRISPR-associated protein, CRISPR/Cas)系统,实现了多次迭代优化,推动了遗传研究的发展和生物育种的升级。甘蔗(Saccharum spp.)是禾本科(Poaceae)重要的C4作物,也是世界上经济价值最高的作物之一。在我国经济作物生产中,甘蔗的地位至关重要:作为主要的糖料作物,它贡献了国内90%的食糖产量;在生物能源领域,甘蔗衍生的乙醇是我国重要的生物燃料[1]。本文简要梳理了植物基因组编辑技术的发展以及甘蔗遗传转化体系的研究,重点介绍了甘蔗基因组学的进展和基因组编辑在甘蔗中的应用,深入探讨了基因组编辑在甘蔗抗倒伏育种中的应用前景,以期为推动基因组编辑在甘蔗育种中的应用提供参考。
1 植物基因组编辑技术的发展
植物基因组编辑通过可编程的序列特异性核酸酶在靶位点上诱导产生DNA双链断裂(double-strand break, DSB),并通过DNA修复途径实现基因组的修饰。目前常用的序列特异性核酸酶主要有3种,分别为ZFNs、TALENs以及CRISPR/Cas系统。
1.1 早期基因组编辑技术
1.1.1 ZFNs
ZFNs是一种人工改造的核酸酶,由含有串联的DNA结合域的转录因子蛋白——锌指蛋白和非特异性核酸内切酶FokⅠ的切割结构域融合构成。通过定向改造ZFN锌指DNA结合域的序列识别特异性,可以实现ZFNs中的DNA结合域特异性识别并结合对应的DNA序列,当2个ZFN单体同各自的目标位点特异结合时,形成具有切割活性的FokⅠ二聚体,在靶位点将DNA切割,进而利用细胞内的非同源末端连接(non-homologous end joining, NHEJ)或同源重组(homologous recombination, HR)等修复机制实现目标基因的靶向敲除(图1A)[2-4]。常用的锌指(zinc-finger, ZF)结构为Cys2-His2锌指,一般由30个氨基酸包裹1个锌原子组成,每个ZF蛋白结构可以特异性地识别并结合3个核酸碱基[5]。研究表明,增加ZF蛋白的数量,ZFN识别靶标DNA序列的长度会得到扩大,从而提高其序列识别特异性[6]。FokⅠ是一种type SⅡ限制核酸酶,并且只在二聚体状态下才具有核酸酶活性。因此针对1个目标位点通常需要设计1对ZFNs,且二者的结合序列间隔区为6−8 bp,从而保证FokⅠ二聚体的形成[7]。2005年,ZFNs介导的基因组编辑技术首次应用于植物,在拟南芥中诱导产生了序列的缺失和插入,并且突变具有可遗传性[8]。随后ZFNs在烟草和玉米等植物中也得到了应用[9]。
1.1.2 TALENs
TALENs技术属于人工改造核酸酶技术,是由类转录因子(transcription activator-like, TAL)效应物的DNA结合结构域和核酸内切酶FokⅠ的切割结构域融合而成的核酸酶。TAL由多个串联重复的单元构成,每个单元通常由33−35个氨基酸组成,并且这些氨基酸高度保守,只有各单元中第12和13位的2个氨基酸是可变的,通常被称为重复可变双残基(repeat variant diresidues, RVDs)[10]。RVDs决定了重复单元的DNA识别特异性:天冬酰胺/异亮氨酸识别A,天冬酰胺/甘氨酸识别T,组氨酸/天冬氨酸识别C,天冬酰胺/天冬酰胺识别G和A,天冬酰胺/赖氨酸识别G[11]。2个TAL单体结合在对应的DNA双链上形成有切割活性的FokⅠ二聚体,在目标位点区进行DNA切割并产生DSB(图1A)[2]。TAL串联重复结构域中的RVDs与靶标DNA序列之间的对应关系使得TAL效应物的串联重复单元可以替换ZFN中的DNA识别元件[4]。与ZFN技术相比,TALENs基因组编辑技术对DNA识别更为特异,靶标位点的设计更为方便,模块组装也更为便捷,因此,在基因组定点编辑领域TALENs被广泛研究和应用。在烟草、水稻等多种植物中,TALENs技术已成功用于基因组编辑[9]。Wang等[12]首次利用TALENs靶标多倍体小麦抗白粉病基因mildew resistance locus O(MLO),导致TaMLO基因的3个拷贝同时突变,从而创制了对白粉病具有广谱抗性的小麦材料。
ZFNs、TALENs均以蛋白质为基础,识别和切割DNA。尽管这2项技术在基因组定点修饰领域带来了突破,但仍存在瓶颈,比如在实施操作过程中技术难度较大、构建组装周期长等,严重限制了其推广应用[2]。
1.2 CRISPR/Cas系统
CRISPR是指规律成簇的间隔短回文重复,是原核生物特有的一种获得性免疫系统[2]。依据Cas蛋白的数量可以将CRISPR/Cas系统分为2类(ClassⅠ和ClassⅡ),ClassⅠ利用多蛋白效应复合物,而ClassⅡ利用单蛋白效应物,基于Cas蛋白的结构和功能可分为6种类型(typeⅠ−Ⅵ)和12种亚型[13-14]。Cas9蛋白是一种核心单酶,目前研究最为广泛的CRISPR/Cas9系统就是在ClassⅡ的基础上发展而来。CRISPR/Cas9系统是在向导RNA(guide RNA, gRNA)引导下招募Cas9蛋白靶向基因组DNA,从而在靶点处产生DSB,诱发细胞内NHEJ和HR修复途径,进而实现对基因组DNA的定点敲除、替换、插入等精准修饰(图1A)[15-17]。其中,NHEJ途径发生频率较高,但通常会在靶点处产生少量碱基的插入或缺失(insertions/deletions, indels),虽然是一种不精确的修复方式,但可以有效地创制基因敲除突变体。HR途径的修复方式更为精确,将人为提供与基因组DNA具有同源序列的供体DNA作为模板进行重组修复,最终实现精准的基因定点替换或定点插入[16,18]。2013年,CRISPR/Cas9系统成功在植物中实现了定点敲除等基因组定点编辑的操作,包括重要农作物水稻、小麦以及模式植物拟南芥和本生烟[19-20]。2022年,Li等[21]利用CRISPR/Cas9系统对多倍体小麦TaMLO基因实现多重编辑,获得了敲除TaMLO-A1和TaMLO-D1并在TaMLO-B1附近产生304 kb大片段删除的突变体,创制了具有广谱白粉病抗性、生长和产量均不受影响的小麦新种质。由于CRISPR/Cas9系统具有构建简单、操作方便、效率高和成本低优势,在生物研究领域和生物育种中被广泛使用。
CRISPR/Cas12a(Cfp1)系统与CRISPR/Cas9系统同属ClassⅡ[22]。Cas12a是一个不仅具有核酸序列特异性还具有DNase和RNase活性的核酸酶[23]。Cas12a通过自身的RNase活性处理前体CRISPR RNA(precursor-CRISPR RNA, pre-crRNA)阵列产生成熟的CRISPR RNA(crRNA)[22]。Cas12a与成熟的crRNA形成复合物并靶向目标DNA,在靶点处通过黏性末端剪切产生DSB,诱发细胞内NHEJ和HR修复途径[23]。与Cas9相比,Cas12a蛋白比来源于化脓性链球菌的Cas9(Cas9 from Streptococcus pyogenes, SpCas9)小,原间隔序列临近序列(protospacer adjacent motif, PAM)偏好T碱基(5′-TTTN-3′),无需反式激活crRNA(trans-activating crRNA, tracrRNA)且crRNA更短。CRISPR/Cas12a系统扩充了基因组编辑靶点的选择范围,并可以通过1个启动子串联多个pre-crRNA阵列,同时进行多个基因的编辑[24]。2017年,Yin等[25]在水稻中应用CRISPR/Cas12a系统成功对类表皮模式因子基因(epidermal patterning factor like 9, EPFL9)进行了编辑。2020年,Liu等[26]在转β葡萄糖苷酸酶基因(β-glucuronidase, GUS)小麦中通过CRISPR/Cas12a靶向单拷贝的GUS基因,成功获得了突变苗。
通过以上研究可以发现,CRISPR/Cas9和CRISPR/Cas12a系统各有特点。Cas9的PAM序列为5′-NGG-3′,而Cas12a的PAM序列则为5′-TTTN-3′,2个系统的靶点选择范围不同。CRISPR/Cas12a可以同时对多个基因进行编辑。而CRISPR/Cas9的编辑效率显著高于CRISPR/Cas12a[26-28],并且CRISPR/Cas9衍生的碱基编辑和引导编辑也具有较高的编辑效率[29-31]。由于甘蔗是复杂的多倍体植物,靶标基因的拷贝数可高达百个[32]。在选择适用于甘蔗的基因组编辑系统时,优先考虑其编辑效率,故CRISPR/Cas9系统及其衍生系统是第一选择。
1.3 基于CRISPR/Cas9系统的精准编辑技术
1.3.1 碱基编辑
DSB引发的HR途径虽然在理论上可实现任意碱基之间的转换,但该途径依赖于特定的细胞类型和细胞周期,加上递送供体DNA到细胞中也是一个问题,因此HR在植物中的应用有限[33]。虽然基因敲除是研究植物基因功能的重要手段,但是研究发现植物中一些单核苷酸点突变是许多重要农艺性状发生变异的遗传基础。于是,基于CRISPR/Cas9系统的碱基编辑技术(base editing, BE)得到开发。碱基编辑系统将只有单链切割活性的Cas蛋白(Cas nickase, nCas, D10A)和可作用于单链DNA(single-stranded DNA, ssDNA)的脱氨酶进行融合,进而实现对目标位点的碱基替换(图1B)[18]。该系统的优点是:不依赖DSB的产生,无需供体DNA,具有高效和广适性[18]。目前根据碱基替换的不同类型可分为胞嘧啶碱基编辑器(cytosine base editor, CBE)、腺嘌呤碱基编辑器(adenine base editor, ABE)、胞嘧啶碱基颠换编辑器(C-to-G base editor, CGBE)和腺嘌呤碱基颠换编辑器(adenine transversion base editor, AYBE)。2016年,Komor等[34]基于来源于小鼠的胞嘧啶脱氨酶(apolipoprotein B mRNA editing enzyme catalytic subunit 1 from rat, rAPOBEC1)、SpCas9切口酶(SpCas9-D10A)及尿嘧啶糖基化酶抑制剂(uracil glycosylase inhibitor, UGI)构建了不产生双链断裂的CBE。2017年,Zong等[35]通过PolⅡ型启动子启动融合rAPOBEC1和UGI的nCas9(D10A)蛋白单元表达,以及通过PolⅢ型启动子启动sgRNA表达,在植物细胞中实现了C-T的碱基编辑。2017年,Gaudelli等[29]利用进化的大肠杆菌tRNA腺苷脱氨酶(tRNA-specific adenosine deaminase from Escherichia coli, ecTadA)融合nCas9(D10A)开发了ABE。2018年,Hua等[36]和Yan等[37]提出相同的ABE改造策略,即引入大肠杆菌中的ecTadA及其高活性突变版本TadA7.10,借助nCas9(D10A)的引导,同时在水稻中成功实现A→T的碱基编辑。2021年,Kurt等[38]以CBE融合尿嘧啶糖基化酶(uracil DNA N-glycosylase, UNG)开发的CGBE可以有效实现C→G的碱基编辑。同年,Sretenovic等[39]基于rAPOBEC1(R33A)融合UNG构建了用于植物的CGBE,在水稻、番茄和杨树中实现了碱基编辑。2023年,Tong等[40]以ABE融合N-甲基嘌呤DNA糖基化酶(N-methylpurine DNA glycosylase, MPG)开发了AYBE,可实现A→Y(Y=C, T)的碱基编辑。同年,Wu等[41]基于哺乳动物细胞中的策略,以ABE融合MPGv3,在水稻中实现了A→K(K=G, T)的碱基编辑。由于植物中的AYBE主要实现A→K的编辑,A→C的编辑效率比较有限,故该系统命名为pAKBE。这4种碱基编辑系统可以在不产生DSB的情况下,分别通过胞嘧啶脱氨酶、改造的腺嘌呤脱氨酶或与CBE/ABE融合的DNA糖基化酶对目标位点特定范围内的胞嘧啶、腺嘌呤进行脱氨基反应或生成无嘧啶/无嘌呤位点,再经DNA修复或复制,最终实现精准的C→T、A→G、C→G、A→T的碱基替换(图1A、1B)。碱基编辑不仅在二倍体植物如水稻和番茄中成功应用,还在多倍体植物中实现了定点突变。2019年,Zhang等[42]通过碱基编辑靶向小麦乙酰乳酸合酶(acetolactate synthase, ALS)和乙酰辅酶A羧化酶(acetyl-coenzyme A carboxylase, ACCase)基因,获得了具有耐除草剂性状的非转基因六倍体小麦。2022年,Wang等[43]在异源四倍体棉花中利用ABE编辑磷脂酰乙醇胺结合蛋白(phosphatidylethanolamine-binding protein, PEBP)基因,成功创制了适宜机械化收获的棉花新种质,并且编辑效率达到64%。综上,碱基编辑在异源多倍体的甘蔗中具有巨大的应用潜力。
1.3.2 引导编辑
2019年,Anzalone等[44]基于莫洛尼鼠白血病病毒逆转录酶(Moloney murine leukemia virus reverse transcriptase, M-MLV RT)融合SpCas9切口酶(SpCas9-H840A)开发了引导编辑系统(prime editing, PE);该系统由2部分构成,即具有单链切割活性的nCas9(H840A)融合M-MLV RT的蛋白分子及引导编辑RNA(prime editing guide RNA, pegRNA)。pegRNA融合了sgRNA、负责结合DNA的结合位点(primer binding site, PBS)以及逆转录模板(reverse transcriptase templates, RTT)(图1C)[45]。PE系统不仅能实现全部类型的碱基替换,还可以进行DNA片段的插入和删除以及不同编辑类型的组合。2020年,Lin等[46]对PE系统的密码子、启动子和编辑条件进行了优化,首次建立了适用于植物的引导编辑(plant prime editing, PPE)系统。在小麦中,Ni等[47]通过优化M-MLV RT活性、添加不同类型的核定位信号等策略开发了升级优化的引导编辑(engineered PPE plus, ePPEplus)系统。在小麦原生质体测试体系中,与PPE系统相比,ePPEplus系统平均编辑效率提高了33.0倍,最高可达18.9%,同时建立了多基因引导编辑(Csy4-mediated multiplex prime editing, CMPE)系统,在小麦原生质体测试体系中实现了4−10个基因的同时编辑,平均效率为7.4%−10.3%,并在小麦转基因植株中实现了2−8个基因的精准编辑。最近,本课题组和合作者共同开发了一种高效且精准的植物基因组大片段DNA操纵技术DualPE(dual prime editing)[31]。该技术利用ePPEplus系统,在目标染色体片段的两端设计靶点,使2个PAM位于目标片段内(PAM-in),从而构建一对反向的3′ DNA flaps,通过精确调控这2个3′ DNA flaps的序列和配对方式,引导细胞内的DNA修复方式发生定向改变,从而实现kb−Mb级染色体片段的精准编辑,包括无缝删除、替换和倒位[31,47]。PE系统已在水稻、小麦、番茄等作物中得到应用,实现了作物新种质的创制[48-49]。PE系统将基因组编辑的精度、尺度和编辑类型的多样性提升到了一个新的水平,在植物育种和功能基因组学研究中具有巨大的应用潜力。
以上研究表明,基因组编辑技术为植物性状的遗传改良开辟了新的途径,使植物遗传改良进入精准设计的阶段。特别是对于多倍体植物而言,基因组编辑突破了传统育种无法实现多拷贝基因编辑的瓶颈。
图1 基因组编辑技术示意图
A:基于序列特异性核酸酶的基因组编辑技术包括ZFNs、TALENs,以及CRISPR/Cas系统;B:碱基编辑;C:引导编辑。
Figure 1 Schematic diagram of genome editing technologies. A: Nuclease-based genome editing technologies that target DNA, including ZFNs, TALENs, and CRISPR/Cas; B: Cytosine base editor, and adenine base editor; C: Prime editor.
Cas: Clustered regularly interspaced short palindromic repeats/CRISPR-associated protein; gRNA: Guide RNA; DSB: Double-strand break; NHEJ: Non-homologous end joining; HR: Homologous recombination; nCas9: Cas9 nickase; UGI: Uracil glycosylase inhibitor; CBE: Cytosine base editor; ABE: Adenine base editor; pegRNA: Prime editing guide RNA.
2 遗传转化体系研究进展
植物遗传转化是借助多种递送方法将外源DNA、RNA、核糖核蛋白复合体(ribonucleoprotein, RNP)等物质导入到生物体细胞中,赋予植物理想的遗传特性来提高产量和抗逆等。甘蔗主要的遗传转化方法有基因枪介导的转化法和农杆菌介导的转化法。
2.1 基因枪介导的甘蔗遗传转化
基因枪介导的转化法是通过高压驱动将包被有外源遗传物质的金属微粒直接递送至植物细胞内,从而实现外源基因的瞬时表达或基因组整合[50]。该方法的优点是可转化的植物种类、组织和细胞范围广,并可一次转化多个载体[51]。然而在使用大量DNA和金属微粒时,该方法可能会导致组织和染色体损伤[52]。
1992年,Bower和Birch[53]首次成功地在甘蔗中进行基因枪介导的转化,通过筛选标记新霉素磷酸转移酶II(neomycin phosphotransferase II, NptII)获得了稳定的转基因甘蔗植株。随后,Bower等[54]通过表达荧光素酶基因(luciferase, LUC)和遗传霉素基因(geneticin, G418),优化了胚性愈伤组织的转化效率,并简化了再生过程。Gallo-Meagher和Irvine[55]在甘蔗胚胎性愈伤组织中表达除草剂抗性基因(bialaphos resistance, Bar),获得了抗除草剂的转基因植株。近年来,基因枪介导的甘蔗遗传转化在甘蔗品种、组织培养条件、DNA浓度和质量、基因枪参数以及轰击后的筛选条件上都做了进一步优化[56-57]。2012年,Taparia等[56]使用不含载体骨架、线性化的最小表达盒(minimal, linear expression cassette, MC),并将MC的一次注射量设置为10 ng,通过基因枪介导转化甘蔗品种‘CP 881762’的未成熟叶轮外植体,在培养起始的12周内获得了稳定转化的甘蔗苗。
2.2 农杆菌介导的甘蔗遗传转化
农杆菌介导的遗传转化技术主要依赖革兰氏阴性土壤杆菌属(Agrobacterium)将Ti质粒的一部分移动并整合到被感染植物细胞核中的天然特性[58],通过根癌农杆菌与发根农杆菌等实现外源基因的有效递送。该方法的优点是能够稳定整合转基因、性价比高,但也存在着许多局限性,如大多数作物对农杆菌具有抗性、转化效率低等[59]。
1998年,Arencibia等[60]首次成功利用农杆菌LBA4404(pTOK233)和EHA101(pMTCA3IG)分别携带超二元载体和超毒菌株,成功获得转化报告基因GUS的甘蔗植株。同年,Enríquez-Obregón等[61]通过根癌农杆菌浸染愈伤组织,将Bar基因导入甘蔗并得到了抗除草剂的甘蔗植株。2014年,Dong等[62]在‘CP72-1210’‘Q208’‘KQ228’‘SP70-1143’‘CP89-2143’‘L99-226’‘L99-233’和‘CP84-1198’这8个甘蔗品种中成功利用农杆菌介导遗传转化,并发现共培养阶段进行干燥处理可以提高转化效率。2017年,Wang等[63]在栽培种甘蔗‘新台糖22号’(‘XTT22’,又称‘ROC22’)中建立了高效的农杆菌介导的转化体系;该体系使用Bar基因作为筛选标记,产生的抗性植株PCR阳性率高达近100%并缩短了组培时间。为了进一步提高甘蔗的转化效率,Sathish等[64]尝试对甘蔗‘CO86032’愈伤组织外源提供多胺(polyamines, PAs),结果显示转化效率提升2倍。这可能是由于外源PAs能促进愈伤组织体细胞胚的诱导、成熟和再生,并且愈伤组织在共培养和补充PAs的再生培养基中再生能力较强。
2.3 其他遗传转化方法
除了传统的基因枪和农杆菌介导的转化方法,研究者们还尝试了其他递送方法。Chen等[65]采用聚乙二醇(polyethylene glycol, PEG)作为转化剂,将线性化载体转化甘蔗原生质体并获得了转基因阳性愈伤组织。Arencibia等[66]使用电穿孔法将含有GUS基因的质粒导入栽培种‘POJ 2878’和‘Ja 60-5’的胚性愈伤组织中,经组织培养后得到转基因阳性的‘Ja 60-5’植株。近期,新兴的递送方法如纳米材料递送系统、病毒介导的递送系统、嫁接转移递送系统、mRNA递送系统被开发并应用于小麦、水稻等作物中[67-70]。新兴递送系统在六倍体小麦中的成功应用尤为值得关注。鉴于小麦与甘蔗均为多倍体作物,前者的技术突破为后者提供了重要参考,预示其在甘蔗遗传转化体系中具有巨大潜力,有望为甘蔗分子育种突破现有瓶颈提供更多可能性。
3 甘蔗基因组学研究进展
基因组序列是基因功能研究的重要基础数据,也是解析作物重要农艺性状形成分子机理和开展全基因组分子设计育种的重要基础。甘蔗育种的材料基础为“甘蔗属复合群”(Saccharum complex),包括甘蔗属及其近缘属。甘蔗属主要包括高贵种(Saccharum officinarum, 2n=80)、割手密(Saccharum spontaneum, 2n=40-128)、中国种(Saccharum sinense, 2n=81-124)、印度种(Saccharum barberi, 2n=111-120)、大茎野生种(Saccharum robustum, 2n=60-200)和食穗种(Saccharum edule, 2n=60-80)[71-72]。甘蔗近缘属包括蔗茅属(Erianthus Michaux.)、芒属(Miscanthus Anderss.)、河八王属(Narenga Bor.)和硬穗茅属(Sclerostachya A.)[72]。其中,高贵种又称热带种,其基因组大小为7.50−8.55 Gb;大茎野生种为7.56−11.78 Gb;割手密为3.36−12.64 Gb;蔗茅为902−937 Mb[73-74]。现代甘蔗栽培品种具有100−130条染色体,75%−85%的基因组来自高贵种,15%−25%来自割手密,5%−10%来自种间重组[75]。由于甘蔗基因组差异较大,在同源多倍体的基础上,还有异源多倍体和非整倍体的特性,导致甘蔗基因组成为世界上最复杂和最具挑战性的基因组之一[76]。
自上世纪90年代开始,巴西、法国、中国、澳大利亚、美国、南非、印度、泰国和哥伦比亚等国家和地区陆续开展甘蔗基因组领域的研究。1999年,美国研究者尝试使用细菌人工染色体(bacterial artificial chromosome, BAC)文库解析甘蔗栽培品种‘R570’的基因组[77]。2003年,巴西多家研究单位合作开展甘蔗基因组表达序列标签(expressed sequence tag, EST)研究;该研究从甘蔗的不同组织中构建了26个标准的cDNA文库并获得高质量转录本,涵盖90%以上的表达基因[78]。由于基因组的复杂性以及测序技术和算法的限制,甘蔗基因组的破译工作进展缓慢。
2018年,福建农林大学研究团队联合多家单位开发了ALLHiC算法,首次实现了同源四倍体甘蔗割手密‘AP85-441’基因组的染色体水平组装[79-80]。该基因组在染色体水平组装的突破,成为甘蔗基因组研究的一个标志性事件。同年,法国研究者联合多国团队发表了栽培种甘蔗‘R570’的一套382 Mb的嵌合单倍型基因组,为栽培种甘蔗基因组的破译提供了基本框架[81]。2019年,中外联合团队共同发表了栽培种甘蔗‘SP80-3280’的基因组草图,首次揭示了甘蔗碳分配的遗传基础,并鉴定了甘蔗中主要的双等位基因变异[82]。2021年,栽培种甘蔗‘CC01-1940’的903.2 Mb的单倍型基因组草图被发布[83]。2022年,野生割手密种甘蔗‘Np-X’的完整基因组被破译,该研究利用基因组学方法系统阐明了甘蔗割手密的起源、染色体基数、基因组倍体、关键性状相关基因的演化,进而提出了解释割手密种复杂遗传背景形成机制的演化模型[84]。同年,泰国研究者发布了首个染色体水平的栽培种甘蔗‘KK3’的基因组草图[85]。2024年,法国主导的多国团队联合发布了栽培种甘蔗‘R570’的多倍体参考基因组,完善了‘R570’的物理遗传图谱[86]。栽培种甘蔗基因组经历了从“基本框架”到“部分染色体”的历程,存在大量嵌合组装并且染色体不完整、序列高度片段化等问题。
2024年,广西大学等单位联合成功破译了栽培种甘蔗‘中蔗1号’(‘ZZ1’)的基因组[87]。该研究采用“基于血缘组分的降维”的组装策略,结合各种测序技术,首次从染色体水平破译栽培种甘蔗,是甘蔗基因组研究的又一个里程碑事件。该研究还初步解析了‘ZZ1’中糖产量和抗病性状的遗传基础,为遗传改良提供了重要理论依据。2025年,广西大学研究团队联合多家单位发布了栽培种甘蔗‘XTT22’染色体水平的基因组,构建了97条染色体,基因组总大小达8.8 Gb,其中95.25%的基因组序列挂载到染色体上[75]。‘XTT22’曾作为我国的主栽品种,是我国90%以上的第四代和第五代甘蔗品种的亲本。该基因组的组装质量和完整性都较高,为现代栽培甘蔗功能基因的挖掘提供了基础性支撑,为我国甘蔗精准育种提供了重要理论指导。
近年来甘蔗近缘种基因组研究不断取得突破。2020−2021年,芒属的芒[88]、南荻(Miscanthus lutarioriparius)[89]和五节芒(Miscanthus floridulus)[90]的基因组相继被破译。2023年,我国研究者发布了蔗茅的基因组[73,91]。甘蔗及其近缘种基因组的破译为甘蔗属复合群的起源和进化提供了更加全面的理解,为挖掘优良农艺性状和抗逆等复杂性状相关基因奠定了基础,对推动现代甘蔗育种技术发展和创制新型育种材料具有重要意义。
4 基因组编辑在甘蔗中的应用
近年来,随着甘蔗基因组的破译,基因组编辑技术逐渐在甘蔗中得到了应用和推广(表1)。2016年,Jung和Altpeter[92]首次通过TALENs基因组编辑技术成功在栽培种甘蔗‘CP88-1762’中敲除木质素生物合成咖啡酸-O-甲基转移酶基因(caffeic acid O-methyltransferase, COMT),获得了木质素含量降低的突变体。深入研究发现,通过单个TALEN对可以将109个COMT基因拷贝中的107个进行编辑,导致突变体的木质素含量降低和木质素单体比值减少,同时糖化效率提高,农艺性状不变[32]。
2021年,Eid等[93]通过靶向叶绿素生物合成相关镁螯合酶亚基基因(magnesium chelatase subunit I, MgCh),首次实现了CRISPR介导的甘蔗基因突变,由于同时编辑的MgCh基因拷贝数不同,敲除突变体叶片颜色由绿到黄色不等,Sanger测序结果显示,59个拷贝中有49个实现了编辑,叶绿素含量减少20%−87%;黄化表型程度与编辑等位基因的数量直接相关,为优化基因组编辑技术提供了直观的表型。Oz等[94]利用CRISPR/Cas9技术在栽培种甘蔗‘CP88-1762’中对ALS基因进行靶向编辑,通过模板介导和HR途径,在11个突变系中引入了2个氨基酸替换(W574L和S653I),赋予突变系除草剂耐受性,平均共编辑频率为2.40%。另外,在25和18个突变系中分别观察到W574L和S653I的单一氨基酸替换,平均编辑效率分别为5.40%和3.90%[94]。2024年,泰国Chanprame团队[95]在栽培种甘蔗‘KK3’中克隆了LIM结构域蛋白基因(LIM domain protein, LIM),并利用CRISPR/Cas9技术将其敲除,从而降低了甘蔗茎中木质素的含量;与野生型相比,敲除突变体的木质素含量减少了9.74%−51.46%,而木质素单体比值升高;同时,木质素合成途径的苯丙氨酸脱氨酶基因(phenylalanine ammonia-lyase, PAL)、肉桂酸-4-羟化酶(cinnamate-4-hydroxylase, C4H)和肉桂醇脱氢酶基因(cinnamyl alcohol dehydrogenase, CAD)的表达随着SoLIM表达量的下调而降低,突变体的细胞壁厚度显著降低。2024年,Brant等[96]报道了CRISPR/Cas9编辑甘蔗的首次田间试验;该团队利用CRISPR/Cas9技术成功对参与调控叶舌和叶耳发育的无叶舌基因(liguleless1, LG1)进行编辑,获得了甘蔗叶倾斜角减小、生物量增加的突变体,为通过优化甘蔗冠层结构以增加光能捕获来提高作物产量奠定了基础;二代测序结果显示,在40个LG1基因拷贝中,共编辑频率为7.40%−100%;其中,一个突变体的共编辑频率为12%,叶片倾斜角度降低了54%,生物量增加了18%。2024年,热带作物生物育种全国重点实验室王勤南团队[97]从甘蔗‘XTT22’克隆获得单倍体关键诱导基因(matrilineal, MTL),该基因在花粉中特异表达;利用CRISPR/Cas9基因组编辑技术靶向ScMTL基因,获得具有8个编辑事件的scmtl突变体,即为甘蔗诱导系T0-1;该诱导系与野生型相比,两者植株形态表型没有明显差异,但是诱导系T0-1花药长度更短,花粉萌发率和种子结实率显著降低;以诱导系T0-1为父本,与甘蔗品种‘粤糖94-128’(2n=109)进行杂交,T0-1在2次独立的杂交实验中获得3株甘蔗单倍体材料(G21-1、G23-1和G23-2),单倍体诱导率在0.59%−0.96%之间。该研究利用基因组编辑创制甘蔗的单倍体诱导系,并通过体内杂交诱导甘蔗栽培品种,成功获得单倍体材料。
以上研究表明,基因组编辑技术在甘蔗基因改造中具有巨大潜力。甘蔗的多倍体特性,使一个基因在甘蔗基因组中存在多个拷贝。在通过基因组编辑产生的甘蔗突变体中,其共编辑效率差别巨大,如LGI基因的突变体成功编辑了3个拷贝,但由于该基因共有40个拷贝,导致共编辑效率只有7.40%(表1),这与六倍体小麦等作物是完全不同的。在甘蔗中,当共编辑的基因拷贝数不同时,会产生剂量效应,获得一系列不同表型的突变体,如MgCh的敲除突变体的叶色由绿到黄,对应编辑的拷贝数由低到高。突变体的表型与共编辑的拷贝数相关,呈梯度变化。与其他作物相比,甘蔗具有精细调整编辑结果的优势。基因组编辑技术为提高甘蔗农艺性状、创制单倍体诱导系以及了解复杂的遗传机制提供了精准的工具。
表1 基因组编辑在甘蔗中的应用
Table 1 Application of genome editing in sugarcane
| Target gene | Genome editing system | Number or percent of co-edited gene copies/alleles | Observed phenotype | Reference |
| --- | --- | --- | --- | --- |
| COMT | TALENs | 8%−99% | 29%−32% lignin reduction | [92] |
| COMT | TALENs | Up to 107/109 | 19.70% lignin reduction, decreased lignin composition (S/G ratio), and up to 43.80% increased saccharification efficiency | [32] |
| MgCh | CRISPR/Cas9 | Up to 49/59 | 20%−87% chlorophyll reduction in leaves | [93] |
| ALS | CRISPR/Cas9 | 3/23 | Nicosulfuron herbicide tolerance | [94] |
| LIM | CRISPR/Cas9 | − | 9.74%−51.46% lignin reduction and increased lignin composition (S/G ratio) | [95] |
| LG1 | CRISPR/Cas9 | Up to 40/40 (7.40%−100%) | 25%−94% reduction in leaf inclination angle, increased 18% (field) to 39% (greenhouse) biomass, increased tiller number, internode number and height | [96] |
| MTL | CRISPR/Cas9 | 4/6 | Decreased anther length and pollen germination rate, 0.59%−0.96% haploid induction rate | [97] |
5 基因组编辑在抗倒伏甘蔗育种中的前景
由于甘蔗的基因组极其复杂并且高多倍化,通过传统育种对其进行遗传改良具有挑战性。甘蔗栽培种在一般生长条件下极难开花,即便开花,种子也大多数是败育的[1]。因此,利用基因组编辑进行甘蔗育种,可以大大加快遗传改良进程。
甘蔗倒伏,会导致产量减少5%−20%,含糖量降低约10%[98]。倒伏发生后,水分和养分的运输受损,光合作用产物减少[99]。倒伏会导致甘蔗的冠层高度降低,机械收获难度和生产成本升高[100]。甘蔗倒伏一般分为茎秆倒伏和根系倒伏[99],与茎秆机械强度、结构性碳水化合物、根系锚固能力及株型结构密切相关。研究表明,抗倒伏品种(如‘GT42’)的茎秆中木质素含量、维管束数量和纤维素含量显著高于全倒伏品种(如‘GF98-296’)[101]。木质素通过增强细胞壁刚性提升茎秆抗弯折能力,而纤维素则通过调控根系发育增强锚固能力。因此,基因组编辑的潜在靶点基因可以从木质素和纤维素合成途径以及根系发育等方面进行挖掘。
5.1 木质素合成途径
木质素是植物苯丙烷代谢途径的产物[102]。由苯丙氨酸脱氨形成肉桂酸,再经过一系列羟基化、甲基化和还原反应,生成木质素的3种主要单体,即H-木质素、G-木质素和S-木质素[103]。苯丙烷代谢途径中主要参与木质素单体合成的酶包括PAL、C4H、4-香豆酸辅酶A连接酶(4-hydroxycinnamate CoA ligase, 4CL)、莽草酸/奎宁酸羟基肉桂酰转移酶(shikimic acid/quinic acid hydroxycinnamoyl transferase, HCT)、香豆酰莽草酸/奎宁酸-3′-羟基化酶(p-coumaroyl shikimate/quinate 3′-hydroxylase, C3′H)、肉桂酰辅酶A还原酶(cinnamoyl-CoA reductase, CCR)、香豆酸-3-羟基化酶(p-coumarate 3-hydroxylase, C3H)、阿魏酸-5-羟基化酶(ferulate 5-hydroxylase, F5H)、COMT、咖啡酰辅酶A-O-甲基转移酶(caffeoyl-CoA O-methyltransferase, CCoAOMT)、CAD、咖啡酰莽草酸酯酶(caffeoyl shikimate esterase, CSE)[104](图2)。
研究发现,在甘蔗中分别降低COMT和4CL的表达量,会导致木质素含量减少和木质素单体比例改变[32,92,105-107]。田间实验结果显示,COMT基因的RNAi植株相较于野生型易发生倒伏[106]。另外,改变CCoAOMT和F5H的表达量只能改变木质素组分,而木质素含量不变[107-108]。这与在高粱[109]和柳枝稷[110]中的结果一致。转录组分析表明,COMT、CCR、CCoAOMT、4CL和PAL分别在高和低纤维基因型甘蔗中差异表达[111]。2023年,Li等[101]通过分析抗倒伏甘蔗品系‘GT42’和全倒伏品系‘GF98-296’的转录组数据发现,在甘蔗的伸长和成熟阶段,CYP84A/F5H、4CL和CAD的表达量在‘GT42’中显著升高,而在‘GF98-296’中受到抑制。在水稻、玉米和高粱中,相较于野生型,cad突变体的木质素含量减少[112-115]。在水稻中,PAL的表达量与木质素含量成正相关[116]。在黑麦草中降低CCR的表达,可以获得低木质素含量的多年生黑麦草[117]。
5.2 纤维素合成途径
纤维素由纤维素合成酶催化合成的β-1,4-糖苷链组成[118]。植物中纤维素合酶(cellulose synthase, CesA)家族在纤维素合成过程中起关键作用。在甘蔗中,转录组分析显示CesA家族含有21个成员,CesA3、CesA4、CesA7、CesA8、CesA10和CesA12在不同时间点显示出更明显的表达量变化,推测这些基因负责次生细胞壁中纤维素的合成[119]。2023年,匡博文等[120]以水稻中纤维素合成基因OsCesA7为参考序列,在甘蔗和其他物种中进行比对并筛选到OsCesA7的同源基因;保守结构域分析结果显示甘蔗CesA7基因中存在纤维素合成相关结构域,转录组分析结果显示甘蔗CesA7基因在栽培种苗期根中表达量显著高于叶,推测该基因参与调控根系发育。2024年,Huang等[121]从甘蔗‘XTT22’叶片中克隆了纤维素合成酶3基因(Ces3)的cDNA序列;SoCes3蛋白与其他植物纤维素合成酶相比具有高活性,并含有植物纤维素合成酶蛋白保守结构域;SoCes3基因在甘蔗的叶、叶鞘和节间表达,其中在节间的表达量最高,特别是第5节间,而叶片中的表达量最低;在烟草中过表达SoCes3,转基因烟草的纤维素和木质素含量增加。
5.3 调控木质素和纤维素合成的转录因子
2018年,澳大利亚Henry团队[111]通过转录组分析发现调控次生细胞壁合成的转录因子在高纤维基因型甘蔗的未成熟和成熟组织中特异性差异表达,这些转录因子包括LIM、MYB、PLATZ、IAA24、bZIP、C2H2和C2C2 DOF锌指家族。2024年,泰国Chanprame团队[95]利用CRISPR/Cas9技术将SoLIM基因敲除,获得了木质素的含量降低、细胞壁厚度下降的突变体。在拟南芥中,MYB转录因子,特别是MYB42、MYB46、MYB61和MYB83,作为主要调控因子参与次生细胞壁的生物合成,并可以直接激活并调控木质素生物合成基因的转录,如PAL、C4H和4CL[122-126]。在水稻中,MYB61通过上调类纤维素合成酶编码基因(strong culm 2, STRONG2)的表达而提高纤维素的合成,从而提升水稻的抗倒伏性状[127]。MYB61的表达量与纤维素含量成正相关,myb61敲除突变体中的纤维素含量下降,细胞壁厚度降低,而MYB61过表达后,CesA4、CesA7和CesA9基因表达量升高,纤维素含量增加[128-129]。转录因子GRF4和NACs分别正调控MYB61的表达,并与赤霉素信号途径中的DELLA蛋白(slender rice 1, SLR1)进行互作[128-130]。
5.4 激素信号通路相关基因
甘蔗DELLA蛋白(GA-insensitive, GAI)是SLR1的同源蛋白,调控甘蔗茎秆发育,过表达ScGAI后植株矮小、分蘖增多,ScGAI表达量降低后株高增加,节间发育早、木质化程度高,但茎秆直径不变[131]。在玉米中,过表达GA20氧化酶基因(GA 20-oxidase 1, GA20ox1)后植株茎长而细,纤维素、木质素和细胞壁残留物增加[132]。在甘蔗中,ScGA20ox的表达量升高会促进甘蔗生长[133]。吲哚乙酸氨基化合成酶基因(gretchen hagen 3, GH3)调控根茎生长,在水稻中过表达OsGH3.8,植株具有更短的根和更少的不定根[134]。在甘蔗中,ScGH3.8已被克隆并证明其编码GH3保守结构域[135]。另外,在水稻中,细胞分裂素氧化酶/脱氢酶基因(cytokinin oxidase/dehydrogenase, CKX2)调控茎秆强度和冠根系统结构,敲除后茎秆变粗,抗倒伏性能增加[136]。
5.5 根系发育相关基因
甘蔗为须根系植物[137],其根系的锚固能力与根系形态相关。在小麦中,TaANR1-TaMADS25模块协同调控木质素合成相关基因的表达以及根系中木质素的积累,其中TaMADS25基因的敲除显著影响小麦主根的发育[138]。在水稻中,葡聚糖内切酶(endo-1,4-beta-glucanase, GLU3)影响根细胞壁的纤维素合成,调节根的伸长,其缺失突变体osglu3具有根部纤维素含量减少、根长降低的表型[139]。水稻生长素外向转运载体基因(PIN-formed 1, PIN1)在维管组织和根原基表达,其缺失突变体ospin1表现出不定根数量显著减少[140]。水稻类YUCCA基因(YUCCA-like, YUCCA1)编码生长素生物合成中的限速酶,过表达该基因会导致水稻冠状根大量增加[141]。目前,有关甘蔗中根系发育基因的研究还有待深入,相关基因还未被克隆。
综上,虽然在挖掘甘蔗抗倒伏性状相关基因方面国内外已获得一定的成果,但是关于甘蔗抗倒伏生物学机制的解析还不够深入,仍需借鉴其他作物的研究,通过基因编辑或过表达创制具有抗倒伏特性的甘蔗新材料。针对木质素和纤维素合成途径的关键基因(COMT、4CL、CCR、PAL和CAD;CesA3、CesA4、CesA7、CesA8和CesA9),转录因子(LIM、MYB、GRF4、NAC和MADS25)以及信号通路相关基因(GA20ox和GH3.8)表达量与木质素和纤维素含量成正相关,可以采用过表达相关基因或通过基因组编辑技术在其启动子区定向插入增强子的方法,提升这些基因的表达量,进而提升甘蔗中木质素和纤维素含量,增强抗倒伏能力。而对于信号通路相关基因(ScGAI和CKX2),则需要利用基因组编辑技术创制敲除突变体,从而增强甘蔗的茎秆强度和根系结构,获得抗倒伏甘蔗新材料。
图2 木质素单体生物合成途径
Figure 2 The monolignol biosynthetic pathway.
PAL: 苯丙氨酸脱氨酶;C4H: 肉桂酸-4-羟基化酶;4CL: 4-香豆酸辅酶A连接酶;CCR: 肉桂酰辅酶A还原酶;CAD: 肉桂醇脱氢酶;C3H: 香豆酸-3-羟基化酶;HCT: 莽草酸/奎宁酸羟基肉桂酰转移酶;C3′H: 香豆酰莽草酸/奎宁酸-3′-羟基化酶;CSE: 咖啡酰莽草酸酯酶;COMT: 咖啡酸/5-羟基阿魏酸-O-甲基转移酶(甘蔗品种‘CP88-1762’中COMT基因有109个拷贝[32]);F5H: 阿魏酸-5-羟基化酶;CCoAOMT: 咖啡酰辅酶A-O-甲基转移酶。
PAL: Phenylalanine ammonia-lyase; C4H: Cinnamate-4-hydroxylase; 4CL: 4-Hydroxycinnamate CoA ligase; CCR: Cinnamoyl-CoA reductase; CAD: Cinnamyl alcohol dehydrogenase; C3H: p-coumarate 3-hydroxylase; HCT: Shikimic acid/quinic acid hydroxycinnamoyl transferase; C3′H: p-coumaroyl shikimate/quinate 3′-hydroxylase; CSE: Caffeoyl shikimate esterase; COMT: Caffeic acid O-methyltransferase (there are 109 COMT copies/alleles in sugarcane cultivar ‘CP88-1762’[32]); F5H: Ferulate 5-hydroxylase; CCoAOMT: Caffeoyl-CoA O-methyltransferase.
6 总结与展望
随着甘蔗基因组的破译,依托基因组信息的基因组编辑在甘蔗中得到了应用和推广。尽管在甘蔗中CRISPR/Cas9研究仍处于早期阶段,但近期发表的研究成果令人对这一技术未来几年的应用充满期待。通过基因组编辑,不仅可以进一步加深对甘蔗不同农艺性状形成的遗传机制和作用机理的理解,还能借鉴其他作物的研究结果,创制抗倒伏能力增强等有利于甘蔗生产的新材料。
精准基因组编辑技术的进步,如BE和PE,为甘蔗改良带来了巨大希望。传统编辑方法受限于NHEJ的不精确性和HR的低效率[142]。BE通过将脱氨酶与Cas9切口酶融合,能够在不造成双链断裂的情况下实现精确的碱基转换[34,143-145]。PE通过将Cas9切口酶与逆转录酶及pegRNA相结合,提供了更高的精确性和灵活性[44,46,48]。这些技术已成功应用于水稻、大豆和小麦等多种作物。尽管大多数关于PE的研究都集中在二倍体物种上,但在六倍体小麦上的成功应用表明其在多倍体作物中的有效性[31,47]。尽管目前尚未在甘蔗中证明BE或PE的有效性,但其在编辑精度和编辑类型多样性上具有巨大潜力。
参考文献
[1] 许孚, 汪洲涛, 路贵龙, 阙友雄. 甘蔗遗传改良中的基因工程: 适用、成就、局限和展望[J]. 农业生物技术学报, 2022, 30(3): 580-593. XU F, WANG ZT, LU GL, QUE YX. Genetic engineering in sugarcane improvement: adaptability, achievements, limitations and prospects[J]. Journal of Agricultural Biotechnology, 2022, 30(3): 580-593 (in Chinese).
[2] 李君, 张毅, 陈坤玲, 单奇伟, 王延鹏, 梁振, 高彩霞. CRISPR/Cas系统: RNA靶向的基因组定向编辑新技术[J]. 遗传, 2013, 35(11): 1265-1273. LI J, ZHANG Y, CHEN KL, SHAN QW, WANG YP, LIANG Z, GAO CX. CRISPR/Cas: a novel way of RNA-guided genome editing[J]. Hereditas, 2013, 35(11): 1265-1273 (in Chinese).
[3] URNOV FD, MILLER JC, LEE YL, BEAUSEJOUR CM, ROCK JM, AUGUSTUS S, JAMIESON AC, PORTEUS MH, GREGORY PD, HOLMES MC. Highly efficient endogenous human gene correction using designed zinc-finger nucleases[J]. Nature, 2005, 435(7042): 646-651.
[4] 刘欢, 孟颖颖, 牛丽芳, 林浩. 基因编辑技术研究进展及其在苜蓿等豆科饲草作物中的应用[J]. 生物工程学报, 2017, 33(10): 1733-1743. LIU H, MENG YY, NIU LF, LIN H. Genome editing technology and its application in forage legumes[J]. Chinese Journal of Biotechnology, 2017, 33(10): 1733-1743 (in Chinese).
[5] PAVLETICH NP, PABO CO. Zinc finger-DNA recognition: crystal structure of a Zif268-DNA complex at 2.1 Å[J]. Science, 1991, 252(5007): 809-817.
[6] MILLER J, McLACHLAN AD, KLUG A. Repetitive zinc-binding domains in the protein transcription factor IIIA from Xenopus oocytes[J]. EMBO Journal, 1985, 4(6): 1609-1614.
[7] BEERLI RR, BARBAS CF. Engineering polydactyl zinc-finger transcription factors[J]. Nature Biotechnology, 2002, 20(2): 135-141.
[8] LLOYD A, PLAISIER CL, CARROLL D, DREWS GN. Targeted mutagenesis using zinc-finger nucleases in Arabidopsis[J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(6): 2232-2237.
[9] MATRES JM, HILSCHER J, DATTA A, ARMARIONÁJERA V, BAYSAL C, HE WS, HUANG X, ZHU CF, VALIZADEH-KAMRAN R, TRIJATMIKO KR, CAPELL T, CHRISTOU P, STOGER E, SLAMETLOEDIN IH. Genome editing in cereal crops: an overview[J]. Transgenic Research, 2021, 30(4): 461-498.
[10] CHEN KL, GAO CX. TALENs: customizable molecular DNA scissors for genome engineering of plants[J]. Journal of Genetics and Genomics, 2013, 40(6): 271-279.
[11] MORBITZER R, RÖMER P, BOCH J, LAHAYE T. Regulation of selected genome loci using de novo-engineered transcription activator-like effector (TALE)-type transcription factors[J]. Proceedings of the National Academy of Sciences of the United States of America, 2010, 107(50): 21617-21622.
[12] WANG YP, CHENG X, SHAN QW, ZHANG Y, LIU JX, GAO CX, QIU JL. Simultaneous editing of three homoeoalleles in hexaploid bread wheat confers heritable resistance to powdery mildew[J]. Nature Biotechnology, 2014, 32(9): 947-951.
[13] MAKAROVA KS, ZHANG F, KOONIN EV. SnapShot: class 1 CRISPR-Cas systems[J]. Cell, 2017, 168(5): 946-946.e1.
[14] MAKAROVA KS, ZHANG F, KOONIN EV. SnapShot: class 2 CRISPR-Cas systems[J]. Cell, 2017, 168(1-2): 328-328.e1.
[15] GASIUNAS G, BARRANGOU R, HORVATH P, SIKSNYS V. Cas9-crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria[J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(39): E2579-E2586.
[16] SYMINGTON LS, GAUTIER J. Double-strand break end resection and repair pathway choice[J]. Annual Review of Genetics, 2011, 45: 247-271.
[17] JINEK M, CHYLINSKI K, FONFARA I, HAUER M, DOUDNA JA, CHARPENTIER E. A programmable dual RNA-guided DNA endonuclease in adaptive bacterial immunity[J]. Science, 2012, 337(6096): 816-821.
[18] 宗媛, 高彩霞. 碱基编辑系统研究进展[J]. 遗传, 2019, 41(9): 777-800. ZONG Y, GAO CX. Progress on base editing systems[J]. Hereditas, 2019, 41(9): 777-800 (in Chinese).
[19] SHAN QW, WANG YP, LI J, ZHANG Y, CHEN KL, LIANG Z, ZHANG K, LIU JX, XI JJ, QIU JL, GAO CX. Targeted genome modification of crop plants using a CRISPR-Cas system[J]. Nature Biotechnology, 2013, 31(8): 686-688.
[20] LI JF, NORVILLE JE, AACH J, McCORMACK M, ZHANG DD, BUSH J, CHURCH GM, SHEEN J. Multiplex and homologous recombination-mediated genome editing in Arabidopsis and Nicotiana benthamiana using guide RNA and Cas9[J]. Nature Biotechnology, 2013, 31(8): 688-691.
[21] LI SN, LIN DX, ZHANG YW, DENG M, CHEN YX, LV B, LI BS, LEI Y, WANG YP, ZHAO L, LIANG YT, LIU JX, CHEN KL, LIU ZY, XIAO J, QIU JL, GAO CX. Genome-edited powdery mildew resistance in wheat without growth penalties[J]. Nature, 2022, 602(7897): 455-460.
[22] ZETSCHE B, GOOTENBERG JS, ABUDAYYEH OO, SLAYMAKER IM, MAKAROVA KS, ESSLETZBICHLER P, VOLZ SE, JOUNG J, van der OOST J, REGEV A, KOONIN EV, ZHANG F. Cpf1 is a single RNA-guided endonuclease of a class 2 CRISPR-Cas system[J]. Cell, 2015, 163(3): 759-771.
[23] DONG D, REN K, QIU XL, ZHENG JL, GUO MH, GUAN XY, LIU HN, LI NN, ZHANG BL, YANG DJ, MA C, WANG S, WU D, MA YF, FAN SL, WANG JW, GAO N, HUANG ZW. The crystal structure of Cpf1 in complex with CRISPR RNA[J]. Nature, 2016, 532(7600): 522-526.
[24] BANDYOPADHYAY A, KANCHARLA N, JAVALKOTE VS, DASGUPTA S, BRUTNELL TP. CRISPR-Cas12a (Cpf1): a versatile tool in the plant genome editing tool box for agricultural advancement[J]. Frontiers in Plant Science, 2020, 11: 584151.
[25] YIN XJ, BISWAL AK, DIONORA J, PERDIGON KM, BALAHADIA CP, MAZUMDAR S, CHATER C, LIN HC, COE RA, KRETZSCHMAR T, GRAY JE, QUICK PW, BANDYOPADHYAY A. CRISPR-Cas9 and CRISPR-Cpf1 mediated targeting of a stomatal developmental gene EPFL9 in rice[J]. Plant Cell Reports, 2017, 36(5): 745-757.
[26] LIU HY, WANG K, JIA ZM, GONG Q, LIN ZS, DU LP, PEI XW, YE XG. Efficient induction of haploid plants in wheat by editing of TaMTL using an optimized Agrobacterium-mediated CRISPR system[J]. Journal of Experimental Botany, 2020, 71(4): 1337-1349.
[27] BERNABÉ-ORTS JM, CASAS-RODRIGO I, MINGUET EG, LANDOLFI V, GARCIA-CARPINTERO V, GIANOGLIO S, VÁZQUEZ-VILAR M, GRANELL A, ORZAEZ D. Assessment of Cas12a-mediated gene editing efficiency in plants[J]. Plant Biotechnology Journal, 2019, 17(10): 1971-1984.
[28] MALZAHN AA, TANG X, LEE K, REN QR, SRETENOVIC S, ZHANG YX, CHEN HQ, KANG M, BAO Y, ZHENG XL, DENG KJ, ZHANG T, SALCEDO V, WANG K, ZHANG Y, QI YP. Application of CRISPR-Cas12a temperature sensitivity for improved genome editing in rice, maize, and Arabidopsis[J]. BMC Biology, 2019, 17(1): 9.
[29] GAUDELLI NM, KOMOR AC, REES HA, PACKER MS, BADRAN AH, BRYSON DI, LIU DR. Programmable base editing of A•T to G•C in genomic DNA without DNA cleavage[J]. Nature, 2017, 551(7681): 464-471.
[30] YU XX, HUO GZ, YU JT, LI HY, LI J. Prime editing: its systematic optimization and current applications in disease treatment and agricultural breeding[J]. International Journal of Biological Macromolecules, 2023, 253: 127025.
[31] ZHAO YD, HUANG ZW, ZHOU XM, TENG W, LIU ZH, WANG WP, TANG SJ, LIU Y, LIU J, WANG WX, CHAI LL, ZHANG N, GUO WL, LIU J, NI ZF, SUN QX, WANG YP, ZONG Y. Precise deletion, replacement and inversion of large DNA fragments in plants using dual prime editing[J]. Nature Plants, 2025, 11(2): 191-205.
[32] KANNAN B, JUNG JH, MOXLEY GW, LEE SM, ALTPETER F. TALEN-mediated targeted mutagenesis of more than 100 COMT copies/alleles in highly polyploid sugarcane improves saccharification efficiency without compromising biomass yield[J]. Plant Biotechnology Journal, 2018, 16(4): 856-866.
[33] CHEN KL, WANG YP, ZHANG R, ZHANG HW, GAO CX. CRISPR/Cas genome editing and precision plant breeding in agriculture[J]. Annual Review of Plant Biology, 2019, 70: 667-697.
[34] KOMOR AC, KIM YB, PACKER MS, ZURIS JA, LIU DR. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage[J]. Nature, 2016, 533(7603): 420-424.
[35] ZONG Y, WANG YP, LI C, ZHANG R, CHEN KL, RAN YD, QIU JL, WANG DW, GAO CX. Precise base editing in rice, wheat and maize with a Cas9-cytidine deaminase fusion[J]. Nature Biotechnology, 2017, 35(5): 438-440.
[36] HUA K, TAO XP, YUAN FT, WANG D, ZHU JK. Precise A·T to G·C base editing in the rice genome[J]. Molecular Plant, 2018, 11(4): 627-630.
[37] YAN F, KUANG YJ, REN B, WANG JW, ZHANG DW, LIN HH, YANG B, ZHOU XP, ZHOU HB. Highly efficient A·T to G·C base editing by Cas9n-guided tRNA adenosine deaminase in rice[J]. Molecular Plant, 2018, 11(4): 631-634.
[38] KURT IC, ZHOU RH, IYER S, GARCIA SP, MILLER BR, LANGNER LM, GRÜNEWALD J, JOUNG JK. CRISPR C-to-G base editors for inducing targeted DNA transversions in human cells[J]. Nature Biotechnology, 2021, 39(1): 41-46.
[39] SRETENOVIC S, LIU SS, LI G, CHENG YH, FAN TT, XU Y, ZHOU JP, ZHENG XL, COLEMAN G, ZHANG Y, QI YP. Exploring C-to-G base editing in rice, tomato, and poplar[J]. Frontiers in Genome Editing, 2021, 3: 756766.
[40] TONG HW, WANG XC, LIU YH, LIU NN, LI Y, LUO JM, MA Q, WU DN, LI JY, XU CL, YANG H. Programmable A-to-Y base editing by fusing an adenine base editor with an N-methylpurine DNA glycosylase[J]. Nature Biotechnology, 2023, 41(8): 1080-1084.




