【目的】筛选具有抑制黄嘌呤氧化酶(XOD)活性的乳酸菌,为降低家禽尿酸水平提供参考。【方法】测定26株乳酸菌细胞内容物(CFE)对XOD的体外抑制能力,从中筛选出抑制率较高的菌株进行细胞代谢物(CFS)对XOD抑制率的测定,并对其人工胃肠液耐受性、抗菌药物敏感性、安全性等特性进行评价及分子生物学鉴定。【结果】4株乳酸菌A2、A6、SC、SN的CFE对XOD的抑制率分别为23.41%、27.45%、24.47%、27.23%,CFS对XOD的抑制率分别为14.26%、17.02%、22.34%、19.57%。4株乳酸菌经人工胃肠液处理后的活菌数保持在$10^{8} ext{CFU·mL}^{-1}$以上,对头孢菌素类(头孢哌酮、头孢呋辛)、大环内酯类(红霉素、罗红霉素)、青霉素类(阿莫西林、氨苄西林、青霉素)、恶唑烷酮类(利奈唑胺)抗菌药物敏感;基于16S rDNA序列分析,A2菌株鉴定为副干酪乳杆菌,A6菌株鉴定为植物乳杆菌,SC菌株鉴定为短乳杆菌,SN菌株鉴定为鼠李糖乳杆菌;小鼠分别连续腹腔注射A2、A6、SC、SN菌液两周后,未见死亡及器官病变。【结论】成功筛选出能够抑制XOD活性的4株乳酸菌,其具有良好的益生性和安全性。
关键词:高尿酸血症;乳酸菌;黄嘌呤氧化酶;益生性;安全性
论文《抑制黄嘌呤氧化酶活性乳酸菌的筛选及其安全性分析》发表在《福建农林大学学报(自然科学版)》,版权归《福建农林大学学报(自然科学版)》所有。本文来自网络平台,仅供参考。
高尿酸血症(hyperuricemia, HUA)是由于机体内尿酸生成过多或排泄障碍引起的代谢性疾病,是痛风发生的前提[1]。禽痛风病是由病原微生物、营养代谢等多种原因引起的尿酸在血液中大量积聚,造成关节、内脏和皮下结缔组织发生尿酸盐沉积而引起的一种危害严重的疾病,严重影响养禽业的经济效益[2]。治疗禽痛风病的关键是降低血液尿酸浓度,可以从减少尿酸的生成和促进尿酸排泄入手。其中,黄嘌呤氧化酶(xanthine oxidase, XOD)是促进尿酸生成的关键酶,其可将嘌呤物质(如次黄嘌呤和黄嘌呤)氧化生成尿酸;降低XOD活性,可有效减少尿酸的产生,从而降低血液尿酸浓度[3-4]。
目前,常用于治疗HUA的XOD抑制剂有别嘌醇、托匹司他、非布司他[5],但痛风多伴有肝、肾功能不全,使用上述药物具有一定的副作用,并且存在药物残留等食品安全问题。应用益生菌进行HUA的治疗是当前研究的热点之一,与药物不同,应用益生菌治疗HUA具有无副作用、无药物残留等优点[6]。研究表明,经乳酸菌(如短乳杆菌[7]、鼠李糖乳杆菌[8]、罗伊氏乳杆菌[8]、副干酪乳杆菌[9]、植物乳杆菌[10])干预的患HUA小鼠,体内XOD的含量、活性及血液尿酸水平显著降低。用乳酸菌治疗HUA具有广阔的应用前景,但目前研究多基于菌株降解核苷,关于乳酸菌抑制XOD活性的研究较少。据此,本研究测定乳酸菌株细胞代谢物(cell-free excretory supernatants, CFS)和细胞内容物(cell-free extracts, CFE)对XOD的抑制率,并通过人工胃肠液耐受性和安全性试验对菌株进行评价,筛选出能够抑制XOD活性的菌株,旨在为降低家禽体内尿酸水平及治疗家禽HUA提供参考。
1 材料与方法
1.1 材料
1.1.1 菌株 26株乳酸菌分别来源于健康鹅胃肠道、自然发酵青贮、酸菜和酸奶样品,由黑龙江省农业科学院畜牧兽医分院畜牧环境与微生物研究所保存。
1.1.2 主要试剂 MRS培养基购自青岛海博生物技术有限公司;黄嘌呤、XOD、别嘌醇购自上海阿拉丁生化科技股份有限公司;革兰氏染色试剂盒购自比克曼生物科技有限公司;药敏纸片购自南京全隆生物技术有限公司;细菌DNA提取试剂盒、Premixed Taq、DL2000 DNA Marker购自北京天根生化科技有限公司;人工胃液、肠液购自创峰自动化科技有限公司;其他试剂均为分析纯。
1.2 乳酸菌株对XOD体外抑制能力的评价
1.2.1 乳酸菌株的活化 取26株保存菌种以3%(体积分数)的接种量接种于MRS肉汤培养基上,于37℃下进行厌氧培养,传代培养3次后备用。
1.2.2 CFE、CFS的制备 参考呼静等[11]的方法制备:取$1 × 10^{9} ext{CFU·mL}^{-1}$菌液,超声破碎后离心,收集的上清经0.22μm滤器过滤,即得到CFE,置于-80℃下保存备用;将菌液离心,采用无菌生理盐水对菌体沉淀进行洗涤2次,将菌液重悬并调节活菌数为$1 × 10^{9} ext{CFU·mL}^{-1}$,置于37℃下厌氧培养12h,离心后收集的上清经0.22μm滤器过滤,即得到CFS,置于-80℃下保存备用。
1.2.3 乳酸菌株对XOD体外抑制能力的测定 参考文献[11-12]的方法并略有改动,XOD抑制率测定反应体系如表1所示,体系中XOD的含量为$0.05 ext{U·mL}^{-1}$,黄嘌呤浓度为$2 ext{mmol·L}^{-1}$,别嘌醇质量浓度为$20 mu ext{g·mL}^{-1}$,样品为乳酸菌株的CFE、CFS及别嘌醇。应用酶标仪测定295nm波长处的光密度(D),每间隔30s测定一次,共测定10min至反应结束。样品对XOD的抑制率按下式计算:
$$抑制率/\%=1-frac{(A-B)}{(C-D)} × 100$$
式中,A为含有样品和XOD的阳性试验组的D;B为含有样品、不含XOD的阳性对照组的D;C为含有XOD、不含样品的阴性试验组的D;D为不含XOD和样品的阴性对照组的D。
表1 XOD抑制率测定反应体系(单位:μL)
| 组别 | V(缓冲液) | V(XOD) | V(样品或别嘌醇) | V(黄嘌呤) |
| A | 115 | 20 | 25 | 40 |
| B | 135 | 0 | 25 | 40 |
| C | 140 | 20 | 0 | 40 |
| D | 160 | 0 | 0 | 40 |
1.3 人工胃肠液耐受性的测定
参考Son等[13]的方法,取活化后的菌液1mL加入9mL人工胃液(pH为3.0),置于37℃下进行厌氧培养,0、3h时分别取样进行菌落计数。取上述培养3h后的菌液1mL加入9mL人工肠液(pH为6.8),置于37℃下进行厌氧培养,0、3h时取样进行菌落计数。菌株存活率按下式计算:
$$存活率/\%=frac{3 ext{h活菌数}}{0 ext{h活菌数}} × 100$$
1.4 对抗菌药物敏感性的测定
选取21种抗菌药物进行敏感性测定。在MRS平板上将100μL菌液均匀涂布后放置药敏片,置于37℃下厌氧培养24h后使用游标卡尺测量抑菌圈直径[14]。菌株耐药性和敏感性采用美国临床实验室标准化委员会(CLSI)标准[15]进行判定。
1.5 乳酸菌株的鉴定
1.5.1 生理生化鉴定 取已纯化的待测乳酸菌株划线于MRS平板上,观察单菌落的形态后进行革兰氏染色。挑取单菌落接种于生理生化鉴定管进行糖醇类(蔗糖、核糖、蕈糖、甘露醇、山梨醇、木糖、乳糖、纤维二糖、葡萄糖、果糖、松三糖、七叶苷)发酵试验、过氧化氢试验、硝酸盐还原试验、吲哚试验。
1.5.2 分子生物学鉴定 将纯化菌株接种于MRS肉汤培养基中,置于37℃下厌氧培养24h后获得菌液,按照细菌DNA提取试剂盒说明书的步骤提取细菌基因组DNA。采用通用引物进行菌株16S rDNA的PCR扩增,具体操作步骤及PCR条件参考王家彬等[12]的方法。将扩增后获得的PCR产物送至睿博兴科(哈尔滨)生物技术有限公司测序。测序获得的序列在NCBI网站上进行BLAST比对,使用MEGA11软件采用邻接法(NJ)构建系统进化树,应用iTOL在线工具对进化树进行注释。
1.6 安全性试验
安全性试验经黑龙江省农业科学院畜牧兽医分院学术委员会批准,编号为XMSYFY202310121。将扩大培养的待测菌液于8000r·min⁻¹下离心10min收集菌体,应用无菌生理盐水将菌液重悬并调节活菌数为$1 × 10^{10} ext{CFU·mL}^{-1}$。将20只健康体质量相近的昆明小鼠随机分为5组,每组4只,在每只小鼠的腹腔分别注射4株乳酸菌悬液$200 mu ext{L·d}^{-1}$,以等量无菌生理盐水的腹腔注射作为对照。腹腔注射连续2周后观察每组小鼠的生长状态,记录小鼠死亡数量[16]。
1.7 数据处理
所有试验均平行进行3次,结果取平均值。试验数据采用SPSS26.0软件处理,数据以平均值±标准偏差表示,$P<0.05$表示差异显著。
2 结果与分析
2.1 乳酸菌株对XOD的体外抑制能力
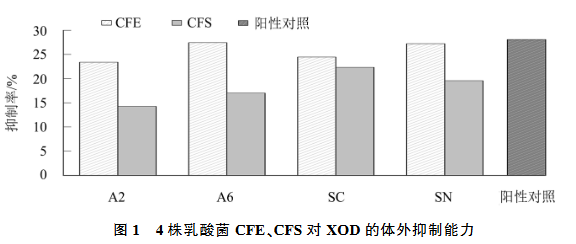
26株乳酸菌的CFE对XOD均具有不同程度的抑制作用,选取抑制率高于20%的乳酸菌株进行CFS对XOD体外抑制能力的测定。选取的4株乳酸菌CFS、CFE对XOD体外抑制能力的测定结果显示:A6、SN菌株的CFE对XOD的抑制率最高,分别为27.45%、27.23%,仅低于阳性对照别嘌醇(28.09%);菌株CFE对XOD整体抑制程度表现为:别嘌醇>A6>SN>SC>A2;菌株CFS对XOD的抑制程度表现为:别嘌醇>SC>SN>A6>A2;SC菌株的CFS对XOD的抑制率最高,为22.34%。整体来看,菌株CFE对XOD的抑制率均高于CFS,表明4株乳酸菌抑制XOD的活性物质主要存在于细胞内。
2.2 乳酸菌株对人工胃肠液的耐受性
试验结果显示,4株菌株经人工胃肠液处理后的活菌数仍能保持在$10^{8} ext{CFU·mL}^{-1}$以上;A2、A6、SC菌株经人工胃肠液处理后的存活率均在90%以上;SN菌株经人工胃肠液处理后的存活率在70%以上。乳酸菌在胃肠道中定殖并发挥作用的前提是活菌数需达到$10^{6} ext{CFU·mL}^{-1}$以上,表明4株乳酸菌均具有良好的胃肠液耐受性,可在胃肠道中定殖并发挥益生功能。
表2 4株乳酸菌经人工胃肠液消化后的活菌数和存活率
| 菌株 | 活菌数/(10⁸ CFU·mL⁻¹) | | | 存活率/% | |
| | 胃液处理0h | 胃液处理3h、肠液处理0h | 肠液处理3h | 胃液 | 肠液 |
| A2 | 1.25±0.08 | 1.32±0.11 | 1.44±0.13 | 105.60±3.21 | 115.65±4.52 |
| A6 | 1.31±0.09 | 1.28±0.10 | 1.29±0.12 | 97.71±2.86 | 99.25±3.18 |
| SC | 1.18±0.07 | 1.12±0.09 | 1.10±0.10 | 94.92±3.05 | 90.15±2.76 |
| SN | 1.23±0.08 | 1.01±0.08 | 0.90±0.07 | 82.11±2.63 | 72.54±2.41 |
注:同行数据后附不同字母者表示同种菌株不同处理之间的差异显著($P<0.05$),附相同字母或无字母者表示差异不显著($P>0.05$)。
2.3 乳酸菌株药敏测定结果
选取21种抗菌药物对4株乳酸菌A2、A6、SC、SN进行药物敏感性测定。结果显示:4株乳酸菌均对头孢菌素类(头孢哌酮、头孢呋辛)、大环内酯类(红霉素、罗红霉素)、青霉素类(阿莫西林、氨苄西林、青霉素)、恶唑烷酮类(利奈唑胺)敏感;对氨基糖苷类(妥布霉素)、β-内酰胺类(氨曲南)表现出耐药;对喹诺酮类(恩诺沙星、诺氟沙星)、氨基糖苷类(丁胺卡那)表现为中度敏感或耐药。
表3 4株乳酸菌药敏测定结果
| 药物名称 | 抑菌圈直径/mm | | | | 耐药性判定 | | | |
| | A2 | A6 | SC | SN | A2 | A6 | SC | SN |
| 丁胺卡那 | 8.39±0.13 | 11.84±0.53 | 16.89±0.12 | 10.57±0.37 | R | R | I | R |
| 克林霉素 | 26.45±0.72 | 13.33±0.49 | 28.35±0.29 | 19.14±0.49 | S | I | S | S |
| 红霉素 | 26.75±0.59 | 20.60±0.82 | 25.31±1.68 | 26.44±0.77 | S | S | S | S |
| 林可霉素 | 19.16±0.69 | 7.20±0.22 | 21.40±1.00 | 17.57±1.63 | S | R | S | S |
| 恩诺沙星 | 13.31±0.44 | 12.68±0.48 | 6.93±0.30 | 16.76±0.28 | I | I | R | I |
| 氨曲南 | 8.46±0.59 | 0.00±0.00 | 0.00±0.00 | 0.00±0.00 | R | R | R | R |
| 罗红霉素 | 22.78±0.62 | 19.54±1.23 | 21.71±0.51 | 26.69±0.54 | S | S | S | S |
| 妥布霉素 | 0.00±0.00 | 7.25±0.30 | 11.41±0.36 | 0.00±0.00 | R | R | R | R |
| 氨苄西林 | 27.09±1.70 | 27.22±0.66 | 27.22±0.52 | 30.14±0.74 | S | S | S | S |
| 阿莫西林 | 23.44±1.70 | 26.48±0.45 | 27.40±0.29 | 30.97±1.10 | S | S | S | S |
| 诺氟沙星 | 11.54±0.84 | 0.00±0.00 | 0.00±0.00 | 15.80±0.84 | R | R | R | I |
| 头孢哌酮 | 26.48±0.38 | 18.85±0.37 | 23.58±0.41 | 32.25±0.31 | S | S | S | S |
| 头孢拉定 | 14.19±0.50 | 22.46±1.09 | 27.24±0.51 | 23.34±1.22 | I | S | S | S |
| 头孢呋辛 | 25.34±0.54 | 17.79±1.06 | 23.45±0.36 | 26.56±0.38 | S | S | S | S |
| 头孢唑林 | 22.60±0.81 | 24.03±0.99 | 25.57±0.73 | 4.24±0.32 | S | S | S | R |
| 头孢他啶 | 18.91±0.67 | 0.00±0.00 | 15.16±0.70 | 25.34±1.86 | S | R | I | S |
| 青霉素 | 19.48±0.49 | 17.80±0.42 | 24.92±0.25 | 23.68±0.58 | S | S | S | S |
| 万古霉素 | 7.58±0.24 | 0.00±0.00 | 22.75±0.40 | 0.00±0.00 | R | R | S | R |
| 利奈唑胺 | 25.01±0.73 | 23.45±0.44 | 28.24±0.52 | 25.93±0.67 | S | S | S | S |
| 美罗培南 | 18.37±0.30 | 19.23±0.32 | 15.17±0.71 | 7.77±0.31 | S | S | I | R |
| 亚胺培南 | 21.08±0.76 | 20.98±0.60 | 18.74±0.21 | 5.36±0.45 | S | S | S | R |
注:S表示敏感,I表示中度敏感,R表示耐药。
2.4 乳酸菌株的鉴定结果
2.4.1 生理生化特性 4株乳酸菌A2、A6、SC、SN在MRS平板上均呈白色、不透明且表面光滑的圆形菌落,菌落边缘规则、无皱褶。染色镜检结果显示:4株乳酸菌染色后呈蓝紫色,均为革兰氏阳性菌,镜检视野下的菌落形态单一,呈短杆状排列。
4株乳酸菌生化鉴定结果显示:4株乳酸菌均能利用蔗糖、蕈糖、葡萄糖、果糖,但不能利用核糖、甘露醇、山梨醇,不产生过氧化氢酶和靛基质,过氧化氢试验、硝酸盐还原试验、吲哚试验均呈阴性。A2、A6、SC菌株均能利用乳糖、七叶苷,但只有SN菌株能利用松三糖。
表4 4株乳酸菌生化鉴定结果
| 菌株 | 糖醇类发酵试验 | | | | | | | | | | | | 过氧化氢试验 | 硝酸盐还原试验 | 吲哚试验 |
| | 蔗糖 | 核糖 | 蕈糖 | 甘露醇 | 葡萄糖 | 松三糖 | 山梨醇 | 木糖 | 乳糖 | 纤维二糖 | 果糖 | 七叶苷 | | | |
| A2 | + | - | + | - | + | - | - | - | + | + | + | + | - | - | - |
| A6 | + | - | + | - | + | - | - | + | + | + | + | + | - | - | - |
| SC | + | - | + | - | + | - | - | + | + | + | + | + | - | - | - |
| SN | + | - | + | - | + | + | - | - | - | - | + | - | - | - | - |
注:+表示阳性或能利用,-表示阴性或不能利用。
2.4.2 分子生物学鉴定结果 4株乳酸菌A2、A6、SC、SN 16S rDNA扩增结果显示:获得4条长度约为1500bp的目的条带。基于16S rDNA序列构建的进化树显示:A2菌株与副干酪乳杆菌(Lactobacillus paracasei)KCKM1014、HBUAS68307的亲缘关系较近,A6菌株与植物乳杆菌(L. plantarum)CMT2的亲缘关系较近,SC菌株与短乳杆菌(L. brevis)2096、1TP03-BL01的亲缘关系较近,SN菌株与鼠李糖乳杆菌(L. rhamnosus)HDB1311表现出较近的亲缘关系。综合NCBI网站上BLAST比对结果和进化关系分析结果,可判断A2菌株属于副干酪乳杆菌,A6菌株属于植物乳杆菌,SC菌株属于短乳杆菌,SN菌株属于鼠李糖乳杆菌。
2.5 安全性试验结果
对照组和4株乳酸菌A2、A6、SC、SN试验组均未有小鼠死亡,小鼠的精神状态、行为活动、饮食及粪便未出现异常,剖检观察未见器官病变,表明A2、A6、SC、SN菌株具有一定的安全性。
3 讨论
禽痛风病危害严重且病因复杂,目前,临床上治疗禽痛风病主要是应用减少尿酸生成的XOD抑制剂(如别嘌醇等),或是促进尿酸排泄的药物(如苯溴马隆、丙磺舒等)[1]。然而,痛风多伴有肝、肾功能不全,上述药物往往伴有严重的不良反应,对肝脏、肾脏具有毒性作用或导致超敏反应[17]。与药物不同,乳酸菌作为一种天然的微生物资源,具有较高的安全性,在预防和控制感染性疾病[18-19]、调节免疫系统[20-21]、提高畜产品质量[22]等方面表现出良好的益生特性。研究表明,摄入乳酸菌可降低机体尿酸含量。如:Wu等[23]从浆水中分离出的发酵乳杆菌JL-3可显著降低小鼠体内尿酸水平,调节HUA引起的肠道菌群紊乱;Kuo等[24]从人体肠道中分离的罗伊氏乳杆菌TSR332和发酵乳杆菌TSF331均能有效降低患HUA小鼠血清和尿液中的尿酸浓度以及血清和肝组织中的XOD活性。上述研究表明,乳酸菌在抑制XOD活性从而减少尿酸生成方面具有广阔的应用前景。
本研究从26株乳酸菌中筛选出4株CFE对XOD的抑制率高于20%的菌株进行CFS对XOD抑制率的测定。结果显示:A6、SN菌株CFE对XOD的抑制率较高,分别为27.45%、27.23%;SC、SN菌株CFS对XOD的抑制率较高,分别为22.34%、19.57%。整体来看,CFE的抑制率均高于CFS,表明4株乳酸菌抑制XOD的活性物质主要存在于细胞内。此结果与王家彬等[12]的研究结果一致。王家彬等[12]研究表明,短乳杆菌LB1lac20的CFE、CFS对XOD的抑制率分别为19.60%、3.90%,CFE与CFS相比具有更高的抑制能力。与此类似,罗伊氏乳杆菌NL02的CFE、CFS对XOD的抑制率均在28.18%以上[11];鼠李糖乳杆菌JY027菌悬液、CFE、CFS对XOD的抑制率分别为85.71%、78.34%、84.05%[25]。上述菌株抑制率差异较大的主要原因是,在XOD体外抑制能力评价试验中,XOD和黄嘌呤的水平不同,XOD含量高,其相应的抑制率也高。呼静等[11]、王家彬等[12]在测定抑制率试验中使用的XOD含量为$0.05 ext{U·mL}^{-1}$,黄嘌呤浓度为$2 ext{mmol·L}^{-1}$,而苗超等[25]使用的XOD含量为$0.20 ext{U·mL}^{-1}$,黄嘌呤浓度为$1.77 ext{mmol·L}^{-1}$。
胃肠液耐受性是益生菌在体内发挥功能的前提[26],也是益生菌最重要的特征之一[27]。本研究中,4株乳酸菌A2、A6、SC、SN经人工胃肠液处理后的存活率为72.54%~115.65%,活菌数仍能保持在$10^{8} ext{CFU·mL}^{-1}$以上,其中副干酪乳杆菌具有良好的胃肠液耐受性且菌落数呈现明显增长的趋势,具有较高的应用价值。Cao等[10]研究表明,植物乳杆菌Q7经人工胃肠液消化后的存活率为99.02%;刘凯龙等[28]研究表明,副干酪乳杆菌经人工胃肠液处理后的活菌数在$10^{8} ext{CFU·mL}^{-1}$以上且存活率为88.60%,与本研究结果一致。
从安全的角度来看,抗生素敏感性是益生菌应用的一个先决条件,因为益生菌可直接或间接地将抗生素抗性基因转移到致病菌中[29]。本研究中,4株乳酸菌A2、A6、SC、SN均对家禽常用抗生素青霉素类(阿莫西林、氨苄西林、青霉素)、头孢菌素类(头孢哌酮、头孢呋辛)敏感。此结果与已报道的副干酪乳杆菌、植物乳杆菌、鼠李糖乳杆菌对阿莫西林、氨苄西林、头孢唑林等抗生素敏感的结果[25,28,30]一致。此外,有研究显示,虽然乳酸菌具有耐药基因,但该编码基因位于染色体上,不具有质粒,表明该耐药基因不会转移到其他细菌中[25,31-32]。
益生菌的安全性是其临床应用的前提[33]。副干酪乳杆菌A2、植物乳杆菌A6、短乳杆菌SC、鼠李糖乳杆菌SN过氧化氢试验、硝酸盐还原试验、吲哚试验均呈阴性。通过连续2周对小鼠腹腔注射活菌液进一步开展安全性评价,对照组和4株乳酸菌A2、A6、SC、SN试验组均未见小鼠死亡,小鼠的状态未出现异常且剖检观察未见器官病变,表明4株乳酸菌具有一定的安全性。本研究仅观察小鼠死亡及器官病变情况,后续将针对不同日龄的家禽饲喂不同剂量的菌液进行全面的安全性评估,以期为A2、A6、SC、SN菌株在临床中的应用提供参考。
4 结论
本研究测定了26株乳酸菌CFE对XOD的体外抑制能力,从中筛选出4株具有良好抑制效果的乳酸菌,分别为副干酪乳杆菌A2、植物乳杆菌A6、短乳杆菌SC、鼠李糖乳杆菌SN。4株乳酸菌CFE对XOD的抑制率表现为A6>SN>SC>A2,CFS对XOD的抑制率表现为SC>SN>A6>A2,且CFE对XOD的抑制率均高于CFS。4株乳酸菌对人工胃肠液具有良好的耐受性,对家禽常用抗生素青霉素、头孢菌素敏感,不产生过氧化氢酶和靛基质;对小鼠行为、状态及饮食、排便无影响,具有一定的安全性。
参考文献
[1]朱坤鹏.一株鹅源唾液乳杆菌的分离及其对雏鹅高尿酸血症的影响[D].长春:吉林大学,2023.
[2]王海鸽,张冰,林志健,等.禽痛风的研究现状与思考[J].动物医学进展,2019,40(8):114-118.
[3]NIU Y F,ZHOU Y F,LIN H,et al.Inhibition of 3,5,2′,4′-tetrahydroxychalcone on production of uric acid in hypoxanthine-induced hyperuricemic mice[J].Biological & Pharmaceutical Bulletin,2018,41(1):99-105.DOI:10.1248/bpb.b1700655.
[4]ZHAO R,CHEN D,WU H L.Pu-erh ripened tea resists to hyperuricemia through xanthine oxidase and renal urate transporters in hyperuricemic mice[J].Journal of Functional Foods,2017,29:201-207.DOI:10.1016/j.jff.2016.12.020.
[5]宋梦瑶,张曦.高尿酸血症的药物治疗[J].医学信息,2021,34(9):58-61.
[6]黄佳豪,李先平,赵军英,等.益生菌缓解高尿酸血症作用机制研究进展[J].食品科学,2023,44(23):282-292.
[7]邓英,何春阳,唐艳,等.短乳杆菌DM9218对高果糖饮食诱导的小鼠高尿酸血症的缓解作用及机制研究[J].中国微生态学杂志,2017,29(12):1387-1390.
[8]倪彩新.乳杆菌对高尿酸血症的影响及作用途径探究[D].无锡:江南大学,2021.
[9]CAO J Y,LIU Q Q,HAO H N,et al.Lactobacillus paracasei X11 ameliorates hyperuricemia and modulates gut microbiota in mice[J].Frontiers in Immunology,2022,13:940228.DOI:10.3389/fimmu.2022.940228.
[10]CAO J Y,BU Y S,HAO H N,et al.Effect and potential mechanism of Lactobacillus plantarum Q7 on hyperuricemia in vitro and in vivo[J].Frontiers in Nutrition,2022,9:954545.DOI:10.3389/fnut.2022.954545.
[11]呼静,崔鹏月,双全.高效降尿酸乳酸菌的筛选及其益生特性研究[J].食品与发酵工业,2022,48(16):150-155.
[12]王家彬,潘力.降解核苷作用乳酸菌的筛选及其潜在降尿酸功能[J].食品科学,2022,43(10):199-206.
[13]SON S H,JEON H L,JEON E B,et al.Potential probiotic Lactobacillus plantarum Ln4 from kimchi:evaluation of β-galactosidase and antioxidant activities[J].LWT-Food Science and Technology,2017,85:181-186.DOI:10.1016/j.lwt.2017.07.018.
[14]寇茜茜,刘荣慧,张伟,等.新疆奶牛乳房炎链球菌的分离鉴定和耐药性分析[J].中国兽医杂志,2023,59(10):76-81.
[15]Clinical Laboratory Standards Institute(CLSI).Performance standards for antimicrobial susceptibility testing:twenty-four informational supplement:M100-S24[S].Wayne,PA:Clinical and Laboratory Standards Institute,2014.
[16]靳胜男,舒慧萍,张冬星,等.猪源生物被膜乳酸菌的筛选、鉴定与体外益生特性评价[J].河南农业科学,2019,48(12):121-127.
[17]STRILCHUK L,FOGACCIF,CICERO A F.Safety and tolerability of available urate-lowering drugs:a critical review[J].Expert Opinion on Drug Safety,2019,18(4):261-271.DOI:10.1080/14740338.2019.1594771.
[18]MESSAOUDI S,MANAIM K,KERGOURLAY G,et al.Lactobacillus salivarius:bacteriocin and probiotic activity[J].Food Microbiology,2013,36(2):296-304.DOI:10.1016/j.fm.2013.05.010.
[19]O'HARA A M,O'REGAN P,FANNING A,et al.Functional modulation of human intestinal epithelial cell responses by Bifidobacterium infantis and Lactobacillus salivarius[J].Immunology,2006,118(2):202-215.DOI:10.1111/j.1365-2567.2006.02358.x.
[20]ZHAI Q X,SHEN X D,CEN S,et al.Screening of Lactobacillus salivarius strains from the feces of Chinese populations and the evaluation of their effects against intestinal inflammation in mice[J].Food & Function,2020,11(1):221-235.DOI:10.1039/C9FO02116G.
[21]ZHANG J H,DENG J,WANG Z S,et al.Modulatory effects of Lactobacillus salivarius on intestinal mucosal immunity of piglets[J].Current Microbiology,2011,62(5):1623-1631.DOI:10.1007/s00284-011-9906-4.
[22]CHAVES B D,BRASHEARS M M,NIGHTINGALE K K.Applications and safety considerations of Lactobacillus salivarius as a probiotic in animal and human health[J].Journal of Applied Microbiology,2017,123(1):18-28.DOI:10.1111/jam.13438.
[23]WU Y,YE Z,FENG P Y,et al.Lactobacillus fermentum JL-3 isolated from "Jiangshui" ameliorates hyperuricemia by degrading uric acid[J].Gut Microbes,2021,13(1):1-18.DOI:10.1080/19490976.2021.1897211.
[24]KUO Y W,HSIEH S H,CHEN J F,et al.Lactobacillus reuteri TSR332 and Lactobacillus fermentum TSF331 stabilize serum uric acid levels and prevent hyperuricemia in rats[J].PeerJ,2021,9:e11209.DOI:10.7717/peerj.11209.
[25]苗超,张宇,杨鑫焱,等.降尿酸乳酸菌菌株的筛选及其全基因组分析[J/OL].中国食品学报.(2023-04-06)[2023-12-05].http://kns.cnki.net/kcms/detail/11.4528.TS.20230406.1332.004.html.
[26]SALEHIZADEH M,MODARRESSIM H,MOUSAVISN,et al.Evaluation of lactic acid bacteria isolated from poultry feces as potential probiotic and its in vitro competitive activity against Salmonella typhimurium[J].Veterinary Research Forum,2020,11(1):67-75.DOI:10.30466/vrf.2018.84395.2110.
[27]LI Y Y,TONG T,LI P F,et al.Screening of potential probiotic Lactobacillaceae and their improvement of type 2 diabetes mellitus by promoting PI3K/AKT signaling pathway in db/db mice[J].Polish Journal of Microbiology,2023,72(3):285-297.DOI:10.33073/pjm-2023-028.
[28]刘凯龙,康小红,张哲,等.副干酪乳杆菌PC-01益生特性和安全性研究[J].中国食品学报,2021,21(11):47-52.
[29]COULIBALY W H,KOUADION R,CAMARA F,et al.Functional properties of lactic acid bacteria isolated from tilapia (Oreochromis niloticus) in Ivory Coast[J].BMC Microbiology,2023,23(1):152.DOI:10.1186/s12866-023-02899-6.
[30]陈晓玉,温敏,张宇,等.犬源益生菌的筛选及特性研究[J/OL].中国饲料.(2023-08-28)[2023-12-15].https://doi.org/10.15906/j.cnki.cn11-2975/s.2023070001-08.
[31]BHUKYA K K,BHUKYA B.Unraveling the probiotic efficiency of bacterium Pediococcus pentosaceus OBK05 isolated from buttermilk:an in vitro study for cholesterol assimilation potential and antibiotic resistance status[J].PLoS ONE,2021,16(11):e0259702.DOI:10.1371/journal.pone.0259702.
[32]FERNANDES M L,PERIN L M,TODOROV S D,et al.In vitro evaluation of the safety and probiotic and technological potential of Pediococcus pentosaceus isolated from sheep milk[J].Semina-Ciencias Agrarias,2018,39(1):113-132.DOI:10.5433/1679-0359.2018v39n1p113.
[33]尹杨燕,潘艳,李小宁,等.1株植物乳杆菌的生物学特性及体外抑菌活性研究[J].中国畜牧兽医,2023,50(2):666-673.




