摘要:目的 观察糖尿病肾病大鼠中NLRP3(NOD-like receptor protein 3)的表达,并在沉默NLRP3和以血管紧张素受体抑制剂(ARB)厄贝沙坦干预后观察NLRP3及炎症和纤维化因子的表达变化,探讨厄贝沙坦对糖尿病肾病大鼠的保护作用。方法 雄性SD大鼠随机分成5组:对照(Control)组、模型(Model)组、空载(Model+Blank)组、NLRP3沉默(Model+NLRP3Sh)组、ARB(Model+ARB)组,分别在糖尿病肾病模型建立后8周、12周处死大鼠并收集肾脏组织。实时荧光定量PCR检测NLRP3、半胱氨酸天冬氨酸蛋白酶-1(Caspase-1)、核因子κB(NF-κB)P65和波形蛋白(Vimentin)的mRNA表达水平;Western blot检测NLRP3、P65、热休克蛋白47(heat shock protein 47,HSP47)和Vimentin的蛋白表达水平;免疫荧光法观察NLRP3、Caspase-1和Vimentin的表达;PAS、PASM和Masson染色观察肾脏病理改变。结果 与对照组比较,模型组及空载组NLRP3、Caspase-1、P65、Vimentin的mRNA表达升高(均P<0.05),NLRP3、Caspase-1、P65、HSP47和Vimentin的蛋白表达升高(均P<0.05);与模型组及空载组相比,沉默组及ARB组的上述指标表达均下调(均P<0.05);模型组与空载组以上指标之间差异无统计学意义。病理染色结果显示,沉默NLRP3和厄贝沙坦干预可减轻糖尿病肾病大鼠肾脏损害,减轻肾小球肥大、肾小球硬化、系膜扩张、间质纤维化。结论 糖尿病肾病大鼠肾脏NLRP3信号通路被激活,且炎性和纤维化因子表达上调。厄贝沙坦可阻断NLRP3信号通路,减轻肾脏损害。天然免疫受体NLRP3可能成为治疗糖尿病肾病的新靶点。
关键词:糖尿病肾病;NLRP3炎症小体;血管紧张素受体阻断剂;肾脏纤维化;天然免疫
论文《厄贝沙坦通过调节NLRP3表达在糖尿病肾病大鼠中的保护作用》发表在《华中科技大学学报(医学版)》,版权归《华中科技大学学报(医学版)》所有。本文来自网络平台,仅供参考。
糖尿病肾病(diabetic nephropathy, DN)是糖尿病常见的严重并发症之一,是终末期肾脏病的主要病因。目前认为糖代谢异常、氧化应激、自噬和天然免疫等是DN进展的重要因素[1]。近年来,天然免疫在DN发生发展中的作用日益受到重视。本课题组前期研究发现天然免疫相关炎症是促进DN发展的关键调控者,高糖状态下肾脏细胞膜上的天然免疫受体TLR4(Toll-like receptor 4)高表达,厄贝沙坦可阻断TLR4信号通路,下调炎性和纤维化因子释放[2-3]。与此同时,越来越多的研究发现细胞质内的天然免疫受体NLRP3也可识别高糖信号,并启动炎症反应[4-5]。因此,深入探讨NLRP3在介导DN天然免疫炎症中的作用十分必要。为进一步探索DN炎症损伤的天然免疫机制,在本研究中,我们通过沉默糖尿病大鼠的NLRP3表达探讨NLRP3在DN发生发展中的作用,并观察厄贝沙坦是否能下调NLRP3并发挥肾脏保护作用。
1 材料与方法
1.1 主要试剂
8周龄SPF级雄性SD大鼠购自长沙天勤生物技术有限公司,实验经南昌大学第一附属医院实验动物伦理委员会批准。链脲佐菌素(Streptozotocin, STZ)(美国Sigma),血糖仪(美国强生),NLRP3沉默慢病毒VL1310-NLRP3-shRNA-3300(上海诺百),厄贝沙坦片(法国赛诺菲),NLRP3抗体(美国ABclonal),Caspase-1抗体(美国Proteintech),P65抗体(美国CST),Vimentin抗体(北京博奥森),HSP47抗体(美国Affinity),β-actin抗体(武汉赛维尔),山羊抗兔IgG二抗(美国ImmunoWay),PAS、PASM、Masson染色试剂盒(北京索莱宝),引物合成(上海生工)。
1.2 动物模型建立
大鼠随机分为对照组(Control组)10只,高糖高脂饮食组40只。喂养4周后,高糖高脂饮食组大鼠于空腹12h后腹腔注射30mg/kg的STZ诱导构建2型糖尿病模型。3d后尾静脉取血,连续检测随机血糖3次,均大于16.7mmol/L则为糖尿病模型建造成功。继续喂养4周,然后将高糖高脂饮食组大鼠随机分为4组,即模型组(Model组)、空载组(Model+Blank组)、NLRP3沉默组(Model+NLRP3Sh组)、血管紧张素受体抑制剂(ARB)组(Model+ARB组)。Model+NLRP3Sh组一次性尾静脉注射2×10⁷ TU NLRP3沉默慢病毒,Model+Blank组注射同剂量空载慢病毒,Model+ARB组按50mg/kg、10mg/mL给予厄贝沙坦溶液灌胃,连续8周。
1.3 大鼠肾脏样本收集
分别在糖尿病模型建造成功4、8、12周后各组分别处死一批大鼠,解剖出双侧肾脏,左肾一半放入4%多聚甲醛溶液内固定,用于PAS、PASM、Masson染色和免疫荧光,另一半用OCT包埋后保存至-80℃冰箱用于免疫荧光检测。右肾同样-80℃保存,一半用于Western blot检测,另一半用于实时荧光定量PCR。
1.4 大鼠肾脏特殊染色
大鼠肾组织在4%多聚甲醛中固定过夜,经石蜡包埋,制成4.5μm的石蜡切片,作PAS、PASM和Masson染色。每只大鼠取3张切片,每张切片于400×光镜下随机选取10个肾小球视野,观察系膜基质增生或肾小球硬化等情况,评估肾小球损伤程度(评分标准:0分无损伤;1分轻度损伤,病变范围<25%;2分中度损伤,病变范围25%~50%;3分重度损伤,病变范围50%~75%;4分极重度损伤,病变范围>75%)。对于染色收集的图像由ImageJ软件计算胶原容积分数,即胶原阳性的蓝色面积与组织总面积的百分比。
1.5 免疫荧光检测
大鼠冰冻切片用4%多聚甲醛固定15min,0.5% Triton X-100通透15min,10%山羊血清封闭1h,滴加一抗4℃过夜,滴加荧光二抗在37℃避光孵育1h,封片、荧光显微镜拍照,收集的图像由ImageJ软件计算平均荧光强度。
1.6 Western blot法
BCA法测定肾脏组织蛋白浓度,统一25μg蛋白上样量,通过SDS-PAGE电泳分离,转移到PVDF膜。5%牛奶封闭1h后加入一抗4℃孵育过夜,与辣根过氧化物酶标记的山羊抗兔二抗孵育1h,然后使用化学发光成像系统进行扫描,实验重复3次。
1.7 实时荧光定量PCR
利用Primer-BLAST设计各基因引物,各引物序列见表1。按照RNA提取试剂盒步骤提取大鼠肾组织RNA并测定浓度,逆转录合成互补cDNA后以β-actin为内参进行PCR扩增,相对表达量采用2⁻ΔΔCt法计算,实验重复3次。
表1 引物序列
Table 1 Primer sequences
| 基因 | 序列 |
| NLRP3 | 上游5'-TGATGAGTGTTCGCTGCAAG-3'
下游5'-GGATCGGAACACAGCCTTTC-3' |
| Caspase-1 | 上游5'-GACCGAGTGGTTCCCTCAAG-3'
下游5'-GACGTGTACGAGTGGGTGTT-3' |
| P65 | 上游5'-TACCACTAAGACGCACCCCA-3'
下游5'-GGCTAATGGCTTGCTCCAGG-3' |
| Vimentin | 上游5'-CGGTTGAAACCAGAGACGGA-3'
下游5'-TTCTACGCCTTTTGGGGGTG-3' |
| β-actin | 上游5'-GTCCACCCGCGAGTACAAC-3'
下游5'-GGATGCCTCTCTTGCTCTGG-3' |
1.8 统计学方法
实验数据采用Graphpad Prism8.0软件进行处理,计量资料以平均值±标准误表示,多组间均数比较采用单因素方差分析,两组间均数比较采用独立样本t检验,以P<0.05表示差异有统计学意义。
2 结果
2.1 DN大鼠模型构建
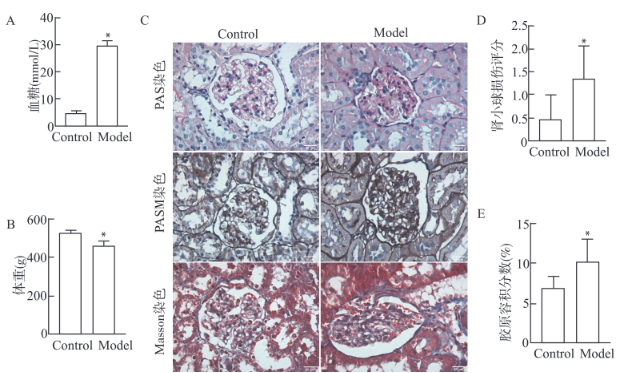
糖尿病模型建立4周后,与对照组相比,模型组大鼠的血糖升高、体重下降(均P<0.05),出现多饮、多食、多尿,对外界刺激的敏感度降低。PAS、PASM染色可见大鼠肾小球肥大,肾小球基底膜增厚,系膜细胞及系膜基质轻度增生,Masson染色可见肾小管间质轻度胶原纤维增生,表明此研究中的大鼠出现了肾脏损害,DN大鼠模型构建成功,见图1。
(图1 糖尿病肾病模型大鼠血糖、体重和肾脏病理改变 Fig.1 Blood glucose, body weight and renal pathological changes in diabetic nephropathy model rats 注:A:造模前后随机血糖比较;B:造模前后体重比较;C:PAS染色(紫红色物质为增生基质);D:PASM染色(黑色物质为增生基质);E:Masson染色(蓝色物质为胶原纤维);F:肾小球损伤评分;G:胶原容积分数;与Control组比较,*P<0.05;n=3)
2.2 DN大鼠肾脏蛋白表达水平变化
Western blot结果显示,与对照组比较,模型组NLRP3、P65蛋白的表达显著升高(均P<0.05),提示糖尿病大鼠肾脏NLRP3炎症小体活化增加。此外,模型组纤维化相关蛋白HSP47和Vimentin的表达也升高(均P<0.05),见图2。
(图2 造模4周后大鼠NLRP3、P65、Vimentin和HSP47蛋白表达水平 Fig.2 Expression levels of NLRP3, P65, Vimentin and HSP47 protein in rats 4 weeks after modeling 注:A:蛋白电泳图;B~E:分别为NLRP3、P65、Vimentin、HSP47蛋白相对表达量统计结果;与Control组比较,*P<0.05;n=3)
2.3 干预后大鼠肾脏NLRP3炎症小体活化情况
沉默NLRP3和厄贝沙坦干预后,在模型建立第8、12周,与对照组比较,模型组及空载组NLRP3、Caspase-1、P65的mRNA或蛋白表达均升高(均P<0.05);与模型组及空载组相比,沉默组及ARB组的上述指标表达均下调(均P<0.05),免疫荧光结果提示糖尿病肾病大鼠肾脏肾小球和肾小管中的NLRP3表达均被抑制。以上结果提示沉默NLRP3和厄贝沙坦干预后DN大鼠肾脏NLRP3炎症小体的激活受到明显抑制,见图3~图5。
(图3 造模8周和12周时各组大鼠NLRP3、Caspase-1、P65和Vimentin mRNA表达水平 Fig.3 The mRNA expression levels of NLRP3, Caspase-1, P65, and Vimentin of rats in each group after 8 and 12 weeks 注:1:Control;2:Model;3:Model+Blank;4:Model+NLRP3Sh;5:Model+ARB;A~D:分别为建模后8周、12周NLRP3、Caspase-1、P65和Vimentin mRNA相对表达量;与Control组比较,*P<0.05;与Model组比较,P<0.05;与Model+Blank组比较,△P<0.05;n=3)
(图4 造模8周和12周时各组大鼠NLRP3、P65、Vimentin和HSP47蛋白表达水平 Fig.4 The protein expression levels of NLRP3, P65, Vimentin and HSP47 of rats in each group after 8 and 12 weeks 注:1:Control;2:Model;3:Model+Blank;4:Model+NLRP3Sh;5:Model+ARB;A:建模后8周蛋白电泳图及相对表达量;B:建模后12周蛋白电泳图及相对表达量;与Control组比较,*P<0.05;与Model组比较,P<0.05;与Model+Blank组比较,△P<0.05;n=3)
(图5 造模8周和12周时各组大鼠肾组织NLRP3、Caspase-1和Vimentin免疫荧光染色结果(×200) Fig.5 Immunofluorescence of NLRP3, Caspase-1 and Vimentin in renal tissue of rats in each group after 8 and 12 weeks (×200) 注:1:Control;2:Model;3:Model+Blank;4:Model+NLRP3Sh;5:Model+ARB;A:免疫荧光染色代表图(绿色为NLRP3阳性、红色为Caspase-1阳性、蓝色为Vimentin阳性);B~D:分别为NLRP3、Caspase-1、Vimentin荧光相对强度统计图;与Control组比较,*P<0.05;与Model组比较,P<0.05;与Model+Blank组比较,△P<0.05;n=3)
2.4 大鼠肾脏损伤和纤维化的情况
造模8周、12周后,肾脏病理检查显示,与对照组比较,模型组及空载组肾脏损伤明显,出现了较严重的系膜细胞和基质增生,肾小球基底膜和肾小囊壁明显增厚,甚至出现肾小球硬化,肾小球内和肾小管间质胶原纤维增生明显。NLRP3沉默组及ARB组肾脏损伤较轻。此外,与对照组比较,模型组及空载组的Vimentin mRNA表达水平明显升高(均P<0.05),HSP47、Vimentin的蛋白表达水平也升高(均P<0.05),而与模型组及空载组相比,NLRP3沉默组及ARB组这些指标的表达均下降,提示沉默NLRP3和厄贝沙坦干预可减轻DN大鼠的肾脏损伤及纤维化,见图6。
(图6 造模8周和12周各组大鼠肾脏病理改变 Fig.6 Pathological changes in kidneys of rats in each group after 8 and 12 weeks 注:1:Control;2:Model;3:Model+Blank;4:Model+NLRP3Sh;5:Model+ARB;A:PAS、PASM和Masson染色(×400);B:肾小球损伤评分;C:胶原容积分数;与Control组比较,*P<0.05;与Model组比较,P<0.05;与Model+Blank组比较,△P<0.05;n=3)
3 讨论
前期研究证实TLR4信号是高糖或高肾素环境下人肾小管上皮细胞天然免疫应答的共同关键通路[2]。近年来,天然免疫受体NLRP3在DN炎症反应过程中的作用日益受到关注。NLRP3是NLRs(NOD-like receptor)家族中的一员,是胞质内的模式识别受体,主要表达于固有免疫细胞,NLRP3炎症小体由NLRP3、凋亡相关斑点蛋白(ASC)和Caspase-1组成[6]。长期高血糖可以诱导肾小球系膜细胞NLRP3和pro-Caspase-1激活表达,释放IL-1β和IL-18,促使肾脏的炎症反应和肾脏胶原纤维的生成增多;NLRP3还能通过与硫氧还蛋白相互作用蛋白(TXNIP)相互作用的方式被激活以启动免疫炎症反应[7-8]。然而,NLRP3参与DN发展的具体机制仍需进一步阐明。
本实验发现,DN大鼠肾组织在第4、8、12周均能检测到NLRP3和NF-κB P65的表达上调,说明高糖可能通过活化NLRP3炎症小体,引起肾脏一系列天然免疫反应,使炎性因子表达增加,这与我们前期的天然免疫研究发现一致[2]。文献报道NLRP3在接触激活信号之前需要启动信号,细胞膜上的Toll样受体识别DAMPs和PAMPs等刺激信号,激活下游NF-κB信号通路,诱导NLRP3、pro-IL-1β、pro-IL-18的转录和翻译,形成NLRP3炎症小体的活化启动信号[9]。沉默DN大鼠NLRP3的表达后,NF-κB P65的表达水平也同时下降,提示NLRP3炎症小体本身也反馈作用于NF-κB信号通路。
为了探讨NLRP3和DN肾脏纤维化的关系,我们选定了HSP47和Vimentin两种纤维化相关蛋白。HSP47与DN患者肾脏中胶原蛋白沉积的增加密切相关[10],对各种小鼠纤维化模型的研究证实敲除HSP47可减少胶原蛋白的积聚并预防纤维化[11-12]。Vimentin是常见的上皮间质转化标志物,在糖尿病大鼠肾小球细胞中可观察到Vimentin表达上调,提示其可能参与了糖尿病患者肾脏间质纤维化的过程[13]。在急性呼吸窘迫综合征模型中,Vimentin可以介导NLRP3炎症小体的活化,继而促进炎症细胞因子IL-18和IL-1β的释放,引起炎症反应[14]。本实验中糖尿病大鼠HSP47、Vimentin表达上调,而沉默NLRP3或者厄贝沙坦干预可以抑制HSP47、Vimentin的表达,肾脏病理检查也显示肾脏纤维化程度减轻,揭示了NLRP3与HSP47、Vimentin及肾脏纤维化存在密切相关性,下调NLRP3及AngⅡ抑制剂可能成为减轻DN肾脏纤维化的新手段。
在前期研究中发现使用厄贝沙坦阻断AngⅡ后可抑制高糖环境中肾脏细胞TLR4的表达[2-3]。AngⅡ是肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system, RAAS)的主要成分,它可以激活抗原呈递细胞来介导促炎活性,启动机体的适应性免疫应答[15-16]。在本研究中,我们发现厄贝沙坦可以抑制NLRP3炎症小体的活化,NLRP3、Caspase-1、NF-κB p65、HSP47、Vimentin的表达均下调,说明厄贝沙坦可以抑制DN大鼠肾脏的炎症反应并减轻纤维化。我们同时在人肾小管上皮细胞模型中也发现了厄贝沙坦这一类似效应(待发表),说明厄贝沙坦可以通过非血流动力学效应对肾脏发挥直接保护作用。
综上所述,DN大鼠模型中,NLRP3表达显著上调,特异性沉默NLRP3或厄贝沙坦干预可以抑制DN大鼠肾脏NLRP3炎症小体的激活和炎症反应,减轻肾脏纤维化。阻断天然免疫NLRP3炎症小体有可能成为延缓DN进展的新策略。
参考文献
[1] Cockwell P, Fisher LA. The global burden of chronic kidney disease[J]. Lancet, 2020, 395(10225): 662-664.
[2] 熊梅梅, 吕柳青, 肖红波, 等. 高糖和血管紧张素Ⅱ对人肾小管上皮细胞Toll样受体4信号表达及炎性和纤维化因子的影响[J]. 中华肾脏病杂志, 2016, 32(1): 43-49.
[3] 吕金雷, 杨玉娟, 吕柳青, 等. siRNA干扰对高糖环境下大鼠肾小管上皮细胞Toll样受体4/转接子髓分化因子88信号通路的影响[J]. 中华肾脏病杂志, 2013, 29(11): 837-841.
[4] Lei Y, Devarapu SK, Motrapu M, et al. Interleukin-1β inhibition for chronic kidney disease in obese mice with type 2 diabetes[J]. Front Immunol, 2019, 10(1223): 1-8.
[5] Bani-hani AH, Leslie JA, Asanuma H, et al. IL-18 neutralization ameliorates obstruction-induced epithelial-mesenchymal transition and renal fibrosis[J]. Kidney Int, 2009, 76(5): 500-511.
[6] He Y, Hara H, Núñez G. Mechanism and regulation of NLRP3 inflammasome activation[J]. Trends Biochem Sci, 2016, 41(12): 1012-1021.
[7] Zhou R, Tardivel A, Thorens B, et al. Thioredoxin-interacting protein links oxidative stress to inflammasome activation[J]. Nat Immunol, 2010, 11(2): 136-140.
[8] Feng H, Gu J, Gou F, et al. High glucose and lipopolysaccharide prime NLRP3 inflammasome via ROS/TXNIP pathway in mesangial cells[J]. J Diabetes Res, 2016, 2016(6973175): 1-11.
[9] Sutterwala FS, Haasken S, Cassel SL. Mechanism of NLRP3 inflammasome activation[J]. Ann N Y Acad Sci, 2014, 1319(1): 82-95.
[10] Kampinga HH, Hageman J, Vos MJ, et al. Guidelines for the nomenclature of the human heat shock proteins[J]. Cell Stress Chaperones, 2009, 14(1): 105-111.
[11] Bellaye PS, Burguy O, Causse S, et al. Heat shock proteins in fibrosis and wound healing: Good or evil?[J]. Pharmacol Ther, 2014, 143(2): 119-132.
[12] Singh K, Agrawal NK, Gupta SK, et al. Decreased expression of heat shock proteins may lead to compromised wound healing in type 2 diabetes mellitus patients[J]. J Diabetes Complications, 2015, 29(4): 578-588.
[13] Ohnuki K, Umezono T, Abe M, et al. Expression of transcription factor Snai1 and tubulointerstitial fibrosis in progressive nephropathy[J]. J Nephrol, 2012, 25(2): 233-239.
[14] Dos Santos G, Rogel MR, Baker MA, et al. Vimentin regulates activation of the NLRP3 inflammasome[J]. Nat Commun, 2015, 6(6574): 1-13.
[15] Benigni A, Cassis P, Remuzzi G. Angiotensin Ⅱ revisited: New roles in inflammation, immunology and aging[J]. EMBO Mol Med, 2010, 2(7): 247-257.
[16] Forrester SJ, Booz GW, Sigmund CD, et al. Angiotensin Ⅱ signal transduction: An update on mechanisms of physiology and pathophysiology[J]. Physiol Rev, 2018, 98(3): 1627-1738.




