目的 探究甲状腺激素通过调节甲亢大鼠卵巢葡萄糖转运,影响黄体增殖、血管生成及凋亡的作用机制。方法 采用随机数字表法将大鼠分为对照组(每日灌胃5mL蒸馏水,$n=5$)和甲亢组(L-甲状腺素250μg/kg溶于5mL蒸馏水后灌胃诱导甲亢,$n=5$)。甲亢诱导第14天处死大鼠,检测卵巢重量、体重,采用放射免疫试剂盒检测血清三碘甲状腺原氨酸(T3)、甲状腺素(T4)、促甲状腺激素(TSH)浓度;检测卵巢组织中葡萄糖转运蛋白Glut1、Glut4的表达,通过免疫组织化学法检测黄体中CDC-47、血管内皮生长因子(VEGF)的表达,采用TUNEL法检测黄体细胞凋亡情况。结果 甲亢组较对照组卵巢重量减轻[(18.79±1.24)g vs.(38.71±4.25)g],差异有统计学意义($P<0.05$),体重[(156.58±24.77)g vs.(147.39±22.15)g]差异无统计学意义($P>0.05$);甲亢组T3[(2.65±0.27)ng/mL]、T4[(48.42±6.37)ng/mL]浓度显著高于对照组,差异有统计学意义($P<0.05$),TSH浓度[(0.54±0.05)ng/mL vs.(0.51±0.04)ng/mL]差异无统计学意义($P>0.05$);甲亢组Glut1蛋白表达低于对照组,Glut4蛋白表达高于对照组,差异均有统计学意义($P<0.05$);甲亢组CDC-47表达的总细胞数[(15.71±2.39)个 vs.(22.43±4.18)个]、黄体细胞数及阳性表达百分比均显著降低,差异有统计学意义($P<0.05$);甲亢组上一周期黄体中VEGF表达百分比[(66.32±5.44)% vs.(50.63±4.13)%]显著升高,新形成黄体中VEGF表达百分比[(76.58±7.18)% vs.(73.24±6.88)%]差异无统计学意义($P>0.05$);甲亢组黄体细胞凋亡量(0.58±0.03 vs.0.31±0.01)显著增加,差异有统计学意义($P<0.05$)。结论 甲状腺激素通过改变黄体的增殖、凋亡及血管生成活性影响大鼠卵巢的寿命和功能,实验性甲亢会降低大鼠黄体增殖活性和血管生成能力,同时促进黄体细胞凋亡。
关键词 甲亢大鼠;甲状腺激素;黄体增殖;血管生成;凋亡
论文《甲状腺激素通过调节甲亢大鼠卵巢葡萄糖转运影响黄体增殖和血管生成、凋亡的机制》发表在《临床和实验医学杂志》,版权归《临床和实验医学杂志》所有。本文来自网络平台,仅供参考。
1 材料与方法
1.1 材料
1.1.1 实验动物 选用健康大鼠,购自三仪动物药品有限公司,许可证号:SYXK(辽)2019,适应性喂养后用于实验。
1.1.2 主要试剂与仪器 L-甲状腺素、免疫组织化学相关试剂盒、ECL试剂盒(上海碧云天生物科技有限公司);放射免疫试剂盒检测T3、T4、TSH;葡萄糖转运蛋白Glut1、Glut4抗体,β-肌动蛋白抗体,CDC-47抗体,VEGF抗体;Olympus BX-40显微镜、Spot Color Insight数码相机、Image ProPlus4.5图像分析软件、TUNEL凋亡检测试剂盒等。
1.1.3 动物分组与模型建立 将大鼠随机分为对照组和甲亢组,每组5只。对照组每日灌胃5mL蒸馏水,甲亢组按250μg/kg剂量灌胃L-甲状腺素溶液,连续14天建立甲亢模型,出现甲亢典型症状后用于后续实验。
1.2 实验方法
1.2.1 标本收集与处理 甲亢诱导第14天处死大鼠,称量体重、卵巢重量,将卵巢组织置于4%中性缓冲甲醛固定液中固定,用于病理切片及免疫组织化学检测;另取部分卵巢组织冻存,用于蛋白表达检测。
1.2.2 血清激素检测 采集大鼠血清,采用放射免疫试剂盒检测T3、T4、TSH浓度,严格按照试剂盒说明书操作,内变异系数<10%。
1.2.3 卵巢组织Glut1、Glut4蛋白表达检测 采用Western blot法。提取卵巢组织总蛋白,Bradford法测定蛋白质浓度,进行SDS-PAGE电泳(10%),电泳转移至硝酸纤维素膜2h,封闭后加入一抗(Glut1 1:1000、Glut4 1:1000、β-肌动蛋白1:10000)孵育,洗膜后加入二抗孵育,ECL化学发光法显色,采用Image Pro Analyzer 4.0分析免疫反应信号,以β-肌动蛋白为内参,计算蛋白相对表达量。
1.2.4 黄体CDC-47、VEGF免疫组织化学检测 卵巢组织石蜡切片,脱蜡至水,抗原修复,封闭后分别加入CDC-47抗体、VEGF抗体孵育,二抗孵育,DAB显色,苏木素复染,脱水透明封片。Olympus BX-40显微镜拍照,Image ProPlus4.5软件计数染色细胞数,计算CDC-47阳性表达细胞数及VEGF表达百分比(%)。
1.2.5 黄体细胞凋亡检测 采用TUNEL测定法。卵巢石蜡切片脱蜡至水,蛋白酶K消化,加入TUNEL反应液孵育,荧光显色,封片后显微镜下观察,Image ProPlus4.5软件定量分析凋亡细胞数量,计算凋亡指数。
1.2.6 统计学方法 采用SPSS软件进行数据分析,计量资料以$�ar{x} pm s$表示,组间比较采用双尾t检验,$P<0.05$为差异有统计学意义。
2 结果
2.1 大鼠体重及卵巢重量变化
甲亢组大鼠卵巢重量较对照组显著减轻,差异有统计学意义($P<0.05$);两组大鼠体重比较,差异无统计学意义($P>0.05$)。
2.2 大鼠血清激素水平变化
甲亢组大鼠血清T3、T4浓度较对照组显著升高,差异均有统计学意义($P<0.05$);两组TSH浓度比较,差异无统计学意义($P>0.05$)。
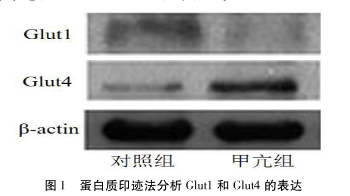
2.3 卵巢组织Glut1、Glut4蛋白表达变化
甲亢组卵巢组织中Glut1蛋白相对表达量显著低于对照组,Glut4蛋白相对表达量显著高于对照组,差异均有统计学意义($P<0.05$)。
2.4 黄体CDC-47表达变化
甲亢组黄体中CDC-47表达的总细胞数、CDC-47表达的黄体细胞数及阳性表达百分比均较对照组显著降低,差异均有统计学意义($P<0.05$)。
2.5 黄体VEGF表达变化
黄体中VEGF表达的百分比面积随着黄体的发育而降低($P<0.05$);甲亢组上一周期黄体中VEGF表达百分比显著高于对照组,差异有统计学意义($P<0.05$);两组新形成的黄体中VEGF表达百分比比较,差异无统计学意义($P>0.05$)。
2.6 黄体细胞凋亡变化
甲亢组黄体细胞凋亡量较对照组显著增加,差异有统计学意义($t=3.545$,$P=0.006$)。
3 讨论
甲状腺激素(TH)参与机体多种生理过程,对胚胎发育、细胞分化及代谢调节至关重要,其水平异常可导致生殖系统功能紊乱。卵泡发育及黄体形成是卵巢生殖功能的核心环节,黄体的增殖、血管生成及凋亡平衡直接影响其功能和寿命,而葡萄糖代谢是黄体细胞增殖、存活的重要物质基础,葡萄糖转运蛋白(Glut)介导的葡萄糖转运是细胞葡萄糖摄取的关键步骤。
本研究发现,实验性甲亢大鼠卵巢重量显著减轻,血清T3、T4水平升高,提示甲亢状态下甲状腺激素异常升高可影响卵巢形态结构。同时,甲亢组卵巢组织Glut1表达降低、Glut4表达升高,表明甲状腺激素可调节卵巢葡萄糖转运蛋白的表达,进而改变卵巢葡萄糖摄取和代谢过程,这可能是甲亢影响卵巢功能的重要机制之一。
黄体增殖活性通过CDC-47表达反映,本研究中甲亢组黄体CDC-47阳性表达显著降低,提示甲亢可抑制黄体细胞增殖,导致黄体增殖活性下降。血管生成是黄体形成和功能维持的关键,VEGF是重要的血管生成因子,本研究发现甲亢组上一周期黄体VEGF表达升高,而新形成黄体VEGF表达无显著变化,推测甲亢状态下甲状腺激素对不同发育阶段黄体的血管生成调节存在差异,可能通过异常调节VEGF表达影响黄体血管生成的时空规律,进而破坏黄体正常结构和功能。
凋亡是黄体退化的重要方式,本研究中甲亢组黄体细胞凋亡量显著增加,表明甲亢可促进黄体细胞凋亡,加速黄体退化。结合葡萄糖转运蛋白的表达变化,推测甲状腺激素通过调节卵巢葡萄糖转运,改变黄体细胞的葡萄糖供应,进而影响黄体细胞的增殖、血管生成及凋亡平衡,最终导致黄体功能异常,影响卵巢整体生殖功能。
甲状腺功能障碍对生殖系统的影响已得到广泛关注,但甲状腺激素调节卵巢黄体功能的具体分子机制尚未完全阐明。本研究揭示了甲状腺激素通过调节葡萄糖转运影响甲亢大鼠黄体增殖、血管生成和凋亡的作用机制,为理解甲状腺功能异常导致的生殖功能紊乱提供了实验依据。但本研究仅在大鼠模型中开展,其结果在人体中的适用性仍需进一步验证,且甲状腺激素调节葡萄糖转运蛋白表达的上游信号通路仍需深入研究。
综上所述,甲状腺激素通过改变黄体的增殖、凋亡及血管生成活性影响大鼠卵巢的寿命和功能,实验性甲亢通过调节卵巢葡萄糖转运蛋白Glut1、Glut4的表达,改变黄体葡萄糖代谢,进而降低黄体增殖活性、异常调节血管生成并促进黄体细胞凋亡,最终导致卵巢功能异常。本研究为甲状腺功能异常相关生殖疾病的发病机制研究和临床干预提供了新的思路和实验基础。
参考文献
[1]谢聪聪,王雪莹,姚冠峰,等.甲状腺激素在卵泡发生中作用的研究进展0].基础医学与临床,2019,39(3):428-433.
[2]Hirai N, Watanabe M, Inoue N. et al. Association of IL -6 gene meth-ylation in peripheral blood cells with the development and prognosis ofautoimmune thyroid diseases []. Autoimmunity, 2019, 52 (7/8) : 251-255.
[3]Wang Q, Ma X, Zhang C. Effects of thyroid hormone on ovarian cellapoptosis in the rat [J]. Reprod Fertil Dev, 2020, 32 (12) : 1060 -1066.
[4]Petranovi e Ov cari cek P, Verburg FA, et al. Higher thyroid hormonelevels and cancer [1]. Eur J Nucl Med Mol Imaging, 2021, 48 (3) :808 -821.
[5]Paunkov A, Chartoumpekis DV, Ziros PG, et al. Impact of AntioxidantNatural Compounds on the Thyroid Gland and Implication of the Keapl /Nr2 Signaling Pathway []. Curr Pharm Des, 2019, 25 (16) : 1828 -1846.
[6]孙婷,甲状腺激素对GLUIT4的影响及其与心磷脂关系的研究[D].厦门:厦门大学,2016.
[7]Schmohl KA, Han Y, Tutter M, et al. Integrin avB3 - dependent thy-roid hormone effects on tumour proliferation and vascularisation []. En-docr Relat Cancer. 2020, 27 (12) : 685 -697.
[8]Schmohl KA, Mueller AM, Dohmann M, et al. Integrin avB3 - Media-ted Effects of Thyroid Hormones on Mesenchymal Stem Cells in TumorAngiogenesis [l]. Thyroid, 2019, 29 (12) : 1843 - 1857.Malagola E, Chen R, Bombardo M, et al. Local hyperthyroidism pro-motes panereatic acinar cell proliferation during acute panereatitis [J]. JPathol, 2019, 248 (2) :217 -229.
[9]Malagola E, Chen R, Bombardo M, et al. Local hyperthyroidism pro-motes panereatic acinar cell proliferation during acute panereatitis [J]. JPathol, 2019, 248 (2):217 -229.
[10]刘东明,严杰,魏瑗,等.甲状腺激素在胎盘发育及局部调控中作用的研究进展.中华妇产科杂志,2021,56(5):364-368.
[11]冯畅,施克新,杨梅,等.甲状腺激素水平与更年期综合征女性情绪障碍程度、性激素水平及免疫功能的相关性分析[].临床和实验医学杂志,2020,19(24):2654-2657.
[12]Ejtahed HS, Angoorani P, Soroush AR, et al. Our Little Friends withBig Roles: Alterations of the Gut Microbiota in Thyroid Disorders [J].Endoer Metab Immune Disord Drug Targets, 2020, 20 (3) : 344 - 350.[13]吴菲,陈俊秀,郑舟琴,等.甲状腺功能正常的2型糖尿病患者甲状腺激素与血糖波动相关性分析].医学研究生学报,2018,31(12):1272 -1275.
[14] Rubingh J, van der Spek A. Fliers E, et al. The Role of Thyroid Hor-mone in the Innate and Adaptive Immune Response during Infection[]. Compr Physiol, 2020, 10 (4) : 1277 -1287.
[15]EI - Eshmawy MM, Shahin M. Thyroid and Eye: Where They Meet inClinical Practice [J]. Endoer Metab Immune Disord Drug Targets,2020,20 (1):39 -49.
[16]Caron P. Thyroid disorders and SARS - CoV -2 infection: from patho-physiological mechanism to patient management LJ]. Ann Endocrinol(Paris), 2020,81 (5):507 -510.
[17] Kalra S, Aggarwal S, Khandelwal D. Thyroid Dysfunction and Type 2Diabetes Mellitus: Screening Strategies and Implications for Management[]. Diabetes Ther, 2019, 10 (6) :2035 -2044.
[18]金鹏锦.NR4A1/2和AdipoR/AMPK在假孕大鼠和猪卵巢黄体中的作用初探[D].南京:南京农业大学,2017.
[19]赵晓妮,汪光荣,游金辉.甲亢患者血浆中VEGF含量测定及相关分析.生物医学工程学杂志,2013,30(2):365-367.




