��������ɢ��Һ����ʳƷ����������Դ��ҽҩ�Ͳ��ϵ�������й㷺��Ӧ�ã������з�����װ�����Լ�˸ߵ���ɢ�Ժ�Ч���Ʊ���Ϊ�ˣ��������ά�����������ɷ���ʵ�ֹ�����ͨ���Եȸ��ܶȼ��ɣ������ü����������˵�����˫����ά���ι�����ͨ������װ��;�ڴ˻�����ʵ���о���Һ���������Լ��ߴ�ֲ����ɡ������ȶ�ģʽ���ǹ���ģʽ��Һ�����ɣ�����4ͨ����8ͨ���������˵�ͨ�����ɵ�Һ�����ԣ�������Ч�ʷֱ��������ͨ���Ľ�4����8����˫��16ͨ����4���������Ʊ���Һ�ε���ɢ�Ժã�����ϵ������3.5%����;������Ч����ߵ���ͨ���Ľ�16�����ɼ���ά���μ��ɹ�����ͨ���ṹ�ܹ��ڱ����Ʊ�Һ�ε���ɢ�Ե�ͬʱ�����Ʊ�Ч�ʡ�
�����ؼ���
����Һ������;����;����;����;��ͨ���Ʊ�;������
�������ġ���ά���μ��ɹ�����ͨ��ʵ��Һ�θ�Ч���ɡ������ڡ�����ѧ��������Ȩ�顶����ѧ�������С�������������ƽ̨�������ο���
��������
����Һ�ι㷺��������Ȼ���ҵ����СҺ�����ڱȱ�����ߡ�Һ���ڻ��Ѹ�١���Ʒ�������͡��ɷ�ֹ�������ơ���ʵ�ָ�ͨ��������ŵ�[1]����ʳƷ[2]������[3]����Դ[4]��ҽҩ[5-6]�Ͳ���[7-8]�������Źؼ�����[9-10]����Ч�ɿص��Ʊ�Һ������㷺���ģӦ�õ�ǰ�ᡣ
������ͳ�Ľ��跨�Ʊ�Һ�ο���ʵ�ָ�Ч�Ʊ�������Һ�γߴ�ֲ���Χ�㡢�ȶ��Ժ��Ʊ��ɿ��Բ�������Һ�γߴ硢�ȶ��Ե��о�ȷҪ���ʵ���ҵӦ��[11-12]������ڽ��跨��Ĥ�黯���ܹ��ɿء��ȶ����Ʊ�����ɢ��Һ�Σ���Һ�γߴ��һ���Ը߶�������Ĥ������״�ľ�ȷ����;���⣬Ĥ�黯����������Ҫ��ܸߣ����ʵ��IJ���������Ӱ��Һ���������������Ĥ�����������ѵ�[13-14]��
���������������ط��Ʊ�Һ�εõ����ٵķ�չ[15]���������������������ɢ�࣬��ɢ����������ļ��м�ѹ�������γɷ�ɢҺ�Ρ��÷������о�ȷ�ɿء��ߴ絥��ɢ�Ժõ�����ŵ㣬�����Ʊ�Ч��ʮ�ֵ���[16]����ˣ��о��ߴ�һ��ʼ��������������ط��Ʊ�Һ�ε�Ч�ʡ�����ߵ���ͨ��Һ������Ƶ���⣬��������Ч�ʵ�����һ�ַ�����������������Һ����������Ŀǰ����ͨ����������������Һ���Ʊ�����������Ҫ�в��С��ֲ�(����)�뻷�εȷ�ʽ�����м���ͨ������һ��ά���ϼ��ɣ������Һ����ͨ����������;�÷�ʽ����ͨ��������Ҫ��̨���黯ʽ[17-19]��T�ʹ���ʽ[20-22]��������[23]�������۽�ʽ[24-27]��ʯ�ε�[28]ͨ����������������ɹ�ʵ��һ�����Ʊ��ߴ��һ�ɿص����ҡ���һ���أ����ǽ�������������ƽ�зŴ�10������ͨ���������У����Ҳ��ʴﵽ0.5 g/h���������Ʊ�Ч��[29]���ü��ɷ�ʽ�������Ͽ�������������ͨ�����������ż���ͨ���������ӣ���ͬͨ��λ�õĶԵ������Ա�֤���������ͨ���������ӣ���Һ�ĵ���ɢ�����Խ��͡��ֲ漯��[30-31]�ֳ����ηֲ漯�ɣ�ÿ�ηֲ潫ͨ��һ��Ϊ�������ɳ̶�����ڲ��нṹ���˽ϴ�������Senn��[32]�������������ͨ�����ɵ�����Һ��������Ч�ʵõ������ߡ�Wang��[33]�о��˷ֲ�Ƕȶ�Һ������ֱ����Բ�ȵ�Ӱ�죬������Һ�ε�����Ч�ʡ�Ŀǰ�ķֲ�ṹ�ֲ�������С��������Ҫ��ηֲ���ܱ�֤�ϴ��������������ɡ�Ȼ���ֲ��������ʹ��ƫ��Ҳ��֮���ӣ�ͬ��ʹ����Һ�ĵ���ɢ���Ա�֤�����μ�����ָ��Һ����ͨ����Բ�����м��ɣ�ͨ��λ�öԵȡ�Nisiako��[34]���û��μ��ɽṹ������128�����ɵ�Ԫ�������ɵ�����Һ�����������ǽ�����װ��ģ�黯���������ɵ�����Һ��������Һ[35]���ü��ɷ�ʽ�ڽϸ�ͨ����������ʱ����ռ���������Խϵ͡�
��������������Ŀǰ���ط��Ʊ�Һ�νṹ�ļ��ɷ�ʽ��Ҫ���ǻ���ƽ�漯�ɣ�����ͨ����ͨ��Ϊn��2ⁿ������һ���̶���������Һ�ε�����Ч�ʣ�����ռ������ʽϵͣ�����ͨ���������ޣ������ż���ͨ���������ӣ�Һ�εĵ���ɢ���½��������ڸ��ɶ��±�֤����Һ�εĵ���ɢ�ԡ���ˣ��dz��б�Ҫ�����µļ��ɽṹ�����Һ�ε�����Ч�ʣ���̽��������Э���ֲ����ɣ�ȷ���Ʊ���Һ�ĸߵ���ɢ�ԡ�
�����ܷ���ʽ��������Һ���ṹ���������������һ�ֻ������ؼ�������ά�����������ɷ���ʵ�ֹ�����ͨ����Ч���Եȼ���;��ά����ʹ��ÿһ���ı������ɴXʮ�����ϰ٣����漶���������ָ������������֤�Ʊ�Ч�ʵļ�������;ÿ����Գƽṹ��ȷ���Ʊ���Һ�ε�ĩ�˽ṹһ�¡�λ�öԵȣ���֤��Һ�εĵ���ɢ�Ըߡ������ü����������˵�����˫����ά������������Һ������װ�ã�����չʵ�������о���ʵ��Һ�ε����ط���Ч�Ʊ�����������̽����ͨ��������������С��Һ������ģʽ������Ч���뵥��ɢ�Ե����ص�Ӱ��;����ѡȡ����������������о�������ά���μ���ͨ����Ϊ4��8ʱ��Һ������Ч����ߴ�ֲ�����;���̽����˫����ά���μ��������µ�Һ������Ч����ߴ�ֲ����ԡ�
����ʵ����Ϻͷ���
����1.1 ʵ��ϵͳ
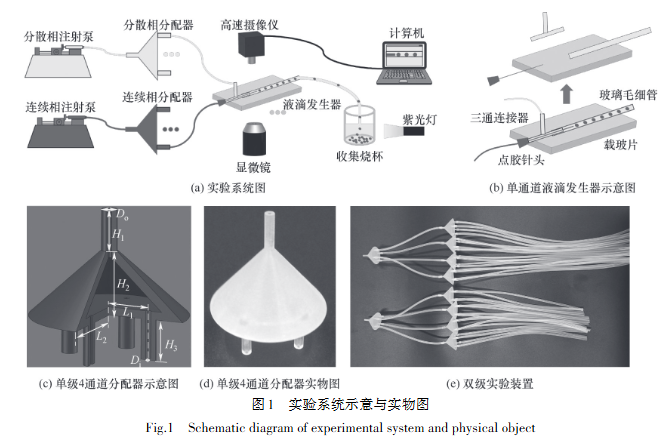
����ʵ��ϵͳ�������������á���������Һ�η��������ռ��ձ��������������������������ȣ���ͼ1(a)��ʾ�����������ڱ��ͷ�ɢ�������������壬�������ڹ�����Һ�η��������������з�ɢ�࣬����Һ�Σ�Һ��ͨ���Ϲ�ƹ̻��ռ���Һ�����ɹ���ͨ�����������Dz����ڼ��������ʾ��
����1.2 ��ͨ��Һ�η�����
��������Һ�η�������Ҫ�����㽺��ͷ����ͨ������������ëϸ�ܡ��ز�Ƭ�����轺�ܺ;��ķ���ϩ�ܡ���ɢ���ˮƽ��������㽺��ͷ�����������ֱ������뵽��ͨ��������;������������ļ�������������֮��Ľ�������ռ������ʱ�������ཫ��ɢ����г�Һ�Ρ�����ͬ������������ѧ�۽����ԺͲ���ëϸ�ܵ���ˮ���ԣ����Ա����ͨ�����������ʪ�Ը��ԡ�
��������Һ�η�������װ���ӿڴ��ߴ������������ƣ������ڳ�������ʱ���ٸ����κβ���������Һ�η�����ԭ��ʾ��ͼ��ͼ1(b)��ʾ��ʵ�����������㽺��ͷ����ͨ������������ëϸ�ܡ��ز�Ƭ�����轺�ܺ;��ķ���ϩ�ܵȷdz���������ȡ;��ͨ��Һ�η�������װ��㣬�ɱ�������֧����ʱ�滻����������ڴ�ͳ�IJ�����Ƕ��װ�ø��Ӽ�㣬������Ҳ�����ι̲����顣
����1.3 ����4ͨ����8ͨ��������
����������ά��ԳƷ�������ʵ��1��n���������������м�������һ�����ڣ��ײ���n��λ�öԵ�(��Գ�)�ij��ڣ����ڵ���ԳƷֲ�ȷ���˸�������������һ��;ͨ���༶��ά��ԳƷ��������ɿ��Խ�Һ���Ʊ�ͨ��������nᵐ(mΪ����������)�����������ľ���ṹ��ͼ1(c)��ʾ�����������ܸ߶�ΪH₁+H₂+H₃=36 mm�����н�������ھ�Ϊ�ھ�Dᵢ=1 mm���⾶D₀=3 mm����H₁=H₃=10 mm�Ŀ���Բ��;�м䲿��Ϊ���ĵ��νṹ���������ӽ��������;�εײ���Բֱ��Ϊ2L₂=30 mm�����ڿ���Բ�������ĵ��εײ�Բ�ĵľ������ȣ�ΪL₁=8 mm��������Ե���������n�ֱ�Ϊ4��8�ķ�������չ�о�������4ͨ��������ʵ��ͼ��ͼ1(d)��ʾ������4ͨ����8ͨ�����������ɼ����ӹ���ã��ɱ��ͣ������ڴ��ģ�ƹ�Ӧ�á�
����1.4 ˫��ʵ��װ��
�����������о�����������Һ���������ԵĻ����ϣ���һ���о�˫����������Һ���������ԣ�̽����ά��ԳƷ�����������Һ�γߴ�������Ƶ�ʵ�Ӱ�졣˫��ʵ��װ����10���ߴ�һ�µ�4ͨ����������װ���ɣ���ͼ1(e)��ʾ�����ù轺�ܽ��в�ͬ����������Һ�η����������ӡ��ʵ������轺�ܵij��ȣ���С�������ߴ�ƫ�������֮��Э��ЧӦ��Ӱ�죬ʹ��ÿ�����ڵ������ֲ����Ӿ��ȡ�
����1.5 ��Һѡȡ������
��������ʵ�����Ʊ�����ҺΪ������Һ��Ϊ�˱��ڷ������ɵ�Һ�εijߴ����ԣ���Һ�ν��й̻���ѡȡ��97%�ļ���������ϩ����(HDDA)��2%�Ĺ�������2-�ǻ�-2-������ͪ��1%�ı�����Լ�Span80���ɵ���Һ��Ϊ��ɢ�࣬��������Ϊ2%�ľ���ϩ��(PVA)ˮ��Һ��Ϊ�����ࡣ��˫��ʵ���У��������������������ѡȡ��������Ϊ0.7%��ϴ�Ӽ���Ϊ�����ࡣ�����Լ�PVA��Span80����Sigma-Aldrich��HDDA����Aladdin��2-�ǻ�-2-������ͪ���յ���B����Macklin��ϴ�Ӽ����Ը߸�����HDDA��һ����ɫ����ɫ����Һ�壬�ǹ�̻�Ϳ�ϵ���Ҫ��ɲ��֣�����UV������ʱ����ɢ���еĹ�������������һ���Ĺ��������Ӷ��������õ����ɻ��������ӣ�����HDDA���巢���̻���������Լ��ܹ����ͽ����������Ӷ�������Һ�ε��������ɡ�ʵ��������������Բ����ܽ����1��ʾ��
������1 ʵ����������
����| ���� | �ܶ�/(kg/m³) | ��/(Pa·s) | ��������/(mN/m) |
����| 2%PVA��Һ | 1013.683 | 0.001498 | 5.08 |
����| 97%HDDA��Һ | 1027.73 | 0.004482 | |
����| 0.7%ϴ�Ӽ���Һ | 1010.16 | 0.000579 | 1.54 |
����1.6 �������
���������е�ÿ��ʵ����ͬ����ʵ���������ظ�4�Σ�������Һ�ε��ռ���ÿ�����ѡȡ100��Һ�ν��н�����������ù�ѧ������������Image View����Һ�γߴ�IJ�����ÿ�β����ظ�3��ȡƽ��ֵ���Լ����˹����������������ñ���ϵ��CV������Һ�γߴ�ĵ���ɢ�ԣ�����ϵ��CVΪҺ�γߴ��ƫ��(STDV)��Һ��ƽ��ֱ��(AD)�ı�ֵ�����㹫ʽ���£�
����ʵ����������
����2.1 ��ͨ��Һ����������
����Ϊ̽��ͨ�����ɶ�Һ������Ч�ʼ�����Һ�ε���ɢ�Ե�Ӱ����ɣ����ڷ����˲�ͬ�����µ�ͨ����Һ������Ч�ʼ���ɢ�ԡ�ѡȡ5������(��ɢ��/������)����ʵ�飬�ֱ�Ϊ0.2/3��0.25/3.75��0.3/4.5��0.35/5.25��0.4/6 ml/min��
����ͼ2չʾ��5�������µ������ֲ���������Һ������Ч�ʼ�����ɢ�Ե�Ӱ�������ӽ�����Կ���������ɢ��/�������������̶��������ȴ�0.2/3 ml/min���ӵ�0.35/5.25 ml/minʱ��Һ��������1052 μm��С��969 μm������Ч�ʽ�����������Һ�εı���ϵ���������ֲ��䣬����2%���ڡ�Һ�α���ϵ����0.35/5.25 ml/min������ͣ���СΪ1.2%��������Ϊ�ڸ������£���������������������Э�����ٽ���Һ�ε��ȶ��γɺ͵���ɢ�Ե����[36]��Ȼ��������ɢ��/����������Ϊ0.4/6 ml/minʱ��Һ�εĵ���ɢ�Ա�Һ�εı���ϵ��ͻ����6.9%��
�������Ľ�һ���۲�����˷�ɢ��/����������Ϊ0.4/6 ml/minʱ��Һ�����ɹ��̣������ͼ3��ʾ����Һ������Ϊ�����ͬ�ߴ�Һ����������ѭ�����̣��������ɵ�Һ�γߴ���С����С���ٽ�ֵ��Һ�γߴ����������ٽ�ֵ������µ�ѭ�����ڣ�Һ�γߴ��ֿ�ʼ��С��������Ϊ���ŷ�ɢ���������������ĵ���������������Ӧ�ӿ죬��ɢ���������ǿ�������������������Һ���γɹ��̴��ڵ������������ɽΡ��ڴ˹����У��϶��������ȼӾ��˾����ľ�����[37]��ʹ�÷�ɢ���쳤�����뱻����λ�������Ա仯�����ɵ�Һ�δ�СҲ���������Ա仯����ʼ�Σ������ڹ����������±��ֳ���ƫ���ڹܹܿ����ƣ���ɢ�౻��������Һ�εļ���λ�ò����ӳ���Һ������ģʽ���ִӵ������������ɵ����ơ����ڷ�ɢ��������δ���ü��γ���ǰһ��Һ���൱����������������ɣ������ɵ�Һ�γߴ���С����ͼ3(a)~(l)��ʾ�����ﵽijһ�ٽ�ֵ����ͼ3(m)��ʾ����ɢ��ټ�����������Һ������ģʽ���ֳ����������������ɵ����ơ���ɢ��������̣�����λ��Ҳ�����̣����ɵ�Һ�γߴ��С�ֿ�ʼ������ֱ������������ͼ3(n)~(r)�������ţ�Һ���ֿ�ʼ��С����ͼ3(r)~(t)��ʾ���Ӷ���������һ��ѭ�����ڡ�Ϊ�˱��ڹ۲��������ͼ3�б�ע��Һ�ε����쳤�ȣ�����λ����Һ��������С��ֵ��ע����ǣ�ÿ�����������ɵ�Һ�δ�С��ͬ�����ɵ�Һ������Ҳ��ͬ������������Һ������С������������ı�����ơ��������ٵ�����ʹ��Һ�����ɴ���һ�����ȶ��Ĺ���״̬��������������֮��Ĺ�������ʱ���������ٵȲ�����С�仯��������Ӱ��Һ�ε����ɹ��̣�ʹ�÷�ɢ�౻���쳤�ȳ��ֳ��������������������̵������Ա仯���Ӷ�����Һ�δ�С����С��������Ķ���������Ҳ�����ؽ�����Ϊ��������Ϊ0.4/6 ml/minʱ��Һ�εı���ϵ���ϸߣ�����ɢ�Խϲ
����2.2 ����4ͨ����8ͨ��Һ����������
�����������о���ͨ��Һ���������ԵĻ����ϣ�̽��������ά����4ͨ����8ͨ��װ�õ�Һ���������ԡ�ѡȡ�˷�ɢ��/�����������ֱ�Ϊ0.2/3 ml/min(����)��0.4/6 ml/min(����)�����ִ����Թ�������ʵ�顣��Ӧ�أ�4ͨ������Ϊ0.8/12 ml/min(����)��1.6/24 ml/min(����)��8ͨ������Ϊ1.6/24 ml/min(����)��3.2/48 ml/min(����)����������뵥ͨ�����жԱȡ�
����2.2.1 ���������������
�����ڢ������������£���ͨ��������4ͨ����8ͨ���Ʊ�Һ�ο��ӻ�ͼ��Һ�εijߴ�ֲ���ͼ4��ʾ����2�����˶�Ӧ������Һ�ε�ƽ������������Ч�ʺͱ���ϵ������ͼ�п��Կ���������ͨ��ʵ�����Ʊ���Һ�γߴ��������1055 μm������ռ�ȷֱ�Ϊ27%��30%��23%�����ҷ�����̬�ֲ�����������������ʹ��Һ�γߴ�ֲ���Χ���������������ɵ�Һ�λ��dz��ֺܺõĵ���ɢ�ԡ��ӱ�2���Կ���������ͨ�������ɵ�Һ�α���ϵ��С������ɢ�Ը�;����ڵ�ͨ��ʵ����(326��/min)������4ͨ����8ͨ��Һ�ε�����Ч�ʷֱ���������ͨ����4��(1301��/min)��8��(2598��/min)��
������2 ��������ʵ������Ҫ��������
����| ͨ���� | ƽ������/μm | ����Ч��/(��/min) | ����ϵ��/% |
����| ��ͨ�� | 1052 | 326 | 1.5 |
����| ����4ͨ�� | 1054 | 1301 | 1.9 |
����| ����8ͨ�� | 1055 | 2598 | 1.9 |
����2.2.2 ���������������
�����ڢ������������£���ͨ����4ͨ����8ͨ���Ʊ�Һ�εĿ��ӻ������ߴ�ֲ���ͼ5��ʾ����3�����˶�Ӧ��Һ������������ڢ��������£�����ʵ�����Ʊ���Һ�γߴ������˫��ֲ�������ʵ����ĵ�һ�������������890 μm�������ڶ�������ֱ������1030��1010��1010 μm����������������Ľ����ȣ�����ʵ�����Ʊ���Һ�ε���ɢ�Բ����ǰ�浥ͨ��Һ�����������о��Ľ��һ�£�˵������4ͨ����8ͨ���������˵�ͨ��Һ�δ�С����С���������Һ���������ԡ�
������3 ��������ʵ������Ҫ��������
����| ͨ���� | ƽ������/μm | ����Ч��/(��/min) | ����ϵ��/% |
����| ��ͨ�� | 956 | 873 | 6.9 |
����| ����4ͨ�� | 957 | 3475 | 6.7 |
����| ����8ͨ�� | 958 | 6944 | 6.6 |
�����������������õ�����ά������������װ���ܹ�ʵ�ָߵ���ɢ��Һ�εĸ�Ч�Ʊ��������ǵ�ͨ�����ɸߵ���ɢ��Һ�εĢ������������ǵ�ͨ������Һ�δ�С����С��������Ģ�������������4ͨ����8ͨ�����ܱ��ֵ�ͨ����Һ���������ԣ���������Ч��Ҳ��Ӧ��������ͨ����4����8����
����2.3 ˫��16ͨ��Һ����������
�����������о�������ά���μ�������Һ���������ԵĻ����ϣ�̽��˫����ά���μ���װ�õ�Һ���������ԡ���ѡȡ��ͨ����ɢ��/�����������ֱ�Ϊ0.1/2��0.1/3��0.2/4��0.2/6 ml/min��4�ֹ�������ʵ�顣��Ӧ�أ�˫��16ͨ������Ϊ1.6/32��1.6/48��3.2/64��3.2/96 ml/min����ͨ����˫��16ͨ����4�������µ������ֲ���ͼ6��ʾ����������̬�ֲ���
�����о���������ڱ�4������ɢ��/�������ͨ�������ֱ�Ϊ0.1/2 ml/minʱ����ͨ��ʵ�����ƽ������Ϊ1032 μm����������Ϊ173��/min������ϵ��Ϊ1.29%;��˫��16ͨ����ƽ������Ϊ1035 μm����������Ϊ2750��/min������ϵ��Ϊ3.33%����ͨ��ʵ������˫��16ͨ��ƽ������ƫ���Ϊ0.3%������ϵ������3.5%���ڣ�������ڵ�ͨ��ʵ���飬˫��16ͨ��������Ч����������ͨ���Ľ�16����
������4 ˫��������Һ���������
����| ��� | ����ͨ����ɢ��/����������/(ml/min) | ��ͨ�� | | | ˫��16ͨ�� | |
����| | | ƽ������/μm | ��������/(��/min) | ����ϵ��/% | ƽ������/μm | ��������/(��/min) | ����ϵ��/% |
����| 1 | 0.1/2 | 1032 | 173 | 1.29 | 1035 | 2750 | 3.33 |
����| 2 | 0.1/3 | 950 | 222 | 1.29 | 948 | 3580 | 2.71 |
����| 3 | 0.2/4 | 925 | 481 | 0.97 | 933 | 7529 | 0.94 |
����| 4 | 0.2/6 | 838 | 646 | 1.34 | 839 | 10391 | 2.30 |
�����������������ŷ�ɢ��/�������ͨ�����������ӣ���ͨ����˫��16ͨ��ʵ�����ƽ����������С;�������ʾ�����;������ϵ����������3.5%���ڣ�˫��16ͨ��ʵ���������Ч�ʾ�Ϊ��ͨ����16���������������ά��ԳƷ��������������ӣ�����Ч����ͨ������Ӧ���ӣ���Һ�εı���ϵ����Ȼ��С�����ɱ����ŵ�ͨ����Һ���������ԡ�
���������������֪�����ñ����������������ʵ�ָߵ���ɢ��Һ�εĸ�Ч�Ʊ�;������ά���μ��ɹ�����ͨ���ṹͨ����������ָ����nⁿ��������Ŀǰ�ѱ����ļ���װ�õ��Ʊ�ͨ�������Ϊn��2ⁿ���������װ�þ����������ơ���װ���Ʊ�Һ�εĵ���ɢ�Գ��������������������������ڷ������ļӹ�ƫ��[38]����ˣ����ż������Ӽ��ӹ�ƫ����ۻ����Ʊ�Һ�εĵ���ɢ���ܻή�ͣ���Լ�Ÿ�װ�õĽ�һ�����ɣ��������Ʊ�Һ��Ч�ʼ����Ǻ���ֵ��̽�������ݡ�
��������
�������������һ�ֻ��ڹ��������ط�����Һ�ε���ά�����������ɹ��ͣ������ü����������˵�����˫����ά������������װ�����ڴ������Ʊ�����ɢ��Һ�Ρ��ڴ˻����ϣ���˿��ӻ�ʵ��ϵͳ�о���ά���μ���������Һ���������ԣ����Ƚ��˲�ͬ���ɶ��µ�Һ���������ԡ���Ҫ�������£�
����1. �ڵ�ͨ��ʵ���У�����ɢ��/�����������Թ̶����ʴ�0.2/3 ml/min���ӵ�0.35/5.25 ml/min��Һ��������С������Ч������Һ�εı���ϵ���������ֲ��䡣������ɢ��/�������������ӵ�0.4/6 ml/min������Һ�����ɴ��ڵ���������֮�����ģʽ�����ִ�СҺ�������Խ������ɣ���������˫���ֲ���
����2. ��ͨ��ƽ����ɢ��/����������Ϊ0.2/3 ml/min�£���ͨ��������4ͨ����8ͨ���Ʊ���Һ�ε���ɢ����Խ������ϵ���ֱ�Ϊ1.5%��1.9%��1.9%;��ͨ��ƽ����ɢ��/����������Ϊ0.4/6 ml/min�£���ͨ��������4ͨ����8ͨ���Ʊ���Һ�ε���ɢ����Խϲ����ϵ���ֱ�Ϊ6.9%��6.7%��6.6%�������ȶ�ģʽ��Һ�����ɻ��ǹ���ģʽ��Һ�����ɣ�4ͨ����8ͨ���������˵�ͨ������Һ�����ԣ�������Ч�ʷֱ��������ͨ���Ľ�4����8�����ɼ�������װ�úܺñ����˵�ͨ����Һ���������ԣ����Ʊ�Ч�ʵõ���Ӧ������
����3. ��ͨ��ƽ����ɢ��/����������Ϊ0.1/2��0.1/3��0.2/4��0.2/6 ml/min�£�˫��16ͨ���Ʊ���Һ�α�����Խ�ĵ���ɢ�ԣ�����ϵ���ֱ�Ϊ3.33%��2.71%��0.97%��2.30%;������Ч���������ͨ���Ľ�16����˫������װ�����ɱ���ԭͨ����Һ���������ԣ�������Ч��ȴ�õ���Ӧ������
�������IJ��ü�����ʵ���˸ߵ���ɢ��Һ�εĸ�Ч�Ʊ���Ϊ���ط���Ч�Ʊ�Һ���ṩ���µ����˼·�������ٽ�Һ�����ؼ����ڸ�������Ľ�һ��Ӧ�á�
��������˵��
����AD��Һ��ƽ��ֱ����μm
����CV������ϵ����%
����(D_i��D_0)���ֱ��Ƿ�������������ڵ��ھ����⾶��mm
����(H_1��H_2��H_3)���ֱ��Ƿ��������ڡ��νṹ�����ڵĸ߶ȣ�mm
����(L_1)�����������ڿ���Բ�������ĵ��νṹ�ײ�Բ�ĵľ��룬mm
����(L_2)���������νṹ�ײ�Բ�뾶��mm
����STDV��Һ�γߴ��ƫ�μm
���������
����[1] Elvira K S, Gielen F, Tsai S S H, et al. Materials and methods for droplet microfluidic device fabrication[J]. Lab on a Chip, 2022, 22(5): 859-875.
����[2] de Oliveira Bianchi J R, de la Torre L G, Costa A L R. Droplet-based microfluidics as a platform to design food-grade delivery systems based on the entrapped compound type[J]. Foods, 2023, 12(18): 3385.
����[3] Yeh S I, Fu C Y, Sung C Y, et al. Microfluidic fabrication of porous PLGA microspheres without pre-emulsification step[J]. Microfluidics and Nanofluidics, 2023, 27(7): 47.
����[4] Xu W, Li X H, Brugger J, et al. Study of the enhanced electricity output of a sliding droplet-based triboelectric nanogenerator for droplet sensor design[J]. Nano Energy, 2022, 98: 107166.
����[5] Cheong D Y, Lee W, Park I, et al. Amyloid formation in nanoliter droplets[J]. International Journal of Molecular Sciences, 2022, 23(10): 5480.
����[6] ��Цӯ, ֣, ������, ��. ���ؿɿ��Ʊ�Һ�Ρ������ͽ��Ҽ���Ӧ��[J]. ����ѧ��, 2024, 75(4): 1455-1468.
����[7] Orbay S, Sanyal A. Molecularly imprinted polymeric particles created using droplet-based microfluidics: preparation and applications[J]. Micromachines, 2023, 14(4): 763.
����[8] ����ͯ, �����, ����Դ, ��. �����Ʊ����������������о���չ[J]. ����ѧ��, 2023, 74(1): 355-364.
����[9] Amirifar L, Besanjideh M, Nasiri R, et al. Droplet-based microfluidics in biomedical applications[J]. Biofabrication, 2022, 14(2): 022001.
����[10] Li B X, Ma X, Cheng J H, et al. Droplets microfluidics platforma tool for single cell research[J]. Frontiers in Bioengineering and Biotechnology, 2023, 11: 1121870.
����[11] Sumitomo S, Ueta M, Uddin M A, et al. Comparison of oil-in-water emulsion between ultrasonic irradiation and mechanical stirring[J]. Chemical Engineering & Technology, 2019, 42(2): 381-387.
����[12] Hoesli C A, Kiang R L J, Raghuram K, et al. Mammalian cell encapsulation in alginate beads using a simple stirred vessel[J]. Journal of Visualized Experiments, 2017(124): 55280.
����[13] Yanagishita T, Inoue T, Kondo T, et al. Preparation of monodisperse LiCoO₂ hollow particles by membrane emulsification using anodic porous alumina[J]. Chemistry Letters, 2018, 47(4): 551-554.
����[14] Zanatta V, Rezzadori K, Penha F M, et al. Stability of oil-in-water emulsions produced by membrane emulsification with microporous ceramic membranes[J]. Journal of Food Engineering, 2017, 195: 73-84.
����[15] Ding Y, Howes P D, DeMello A J. Recent advances in droplet microfluidics[J]. Analytical Chemistry, 2020, 92(1): 132-149.
����[16] Hu C X, Jin K, Ma H B. A universal model for continuous “one-to-two” high-efficient droplet generation in digital microfluidics[J]. Applied Physics Letters, 2023, 122(18): 181601.
����[17] Ofner A, Mattich I, Hagander M, et al. Controlled massive encapsulation via tandem step emulsification in glass[J]. Advanced Functional Materials, 2019, 29(4): 1806821.
����[18] Opalski A S, Makuch K, Lai Y K, et al. Grooved step emulsification systems optimize the throughput of passive generation of monodisperse emulsions[J]. Lab on a Chip, 2019, 19(7): 1183-1192.
����[19] Vladisavljević G T, Ekanem E E, Zhang Z L, et al. Long-term stability of droplet production by microchannel (step) emulsification in microfluidic silicon chips with large number of terraced microchannels[J]. Chemical Engineering Journal, 2018, 333: 380-391.
����[20] Han T T, Zhang L, Xu H, et al. Factory-on-chip: modularised microfluidic reactors for continuous mass production of functional materials[J]. Chemical Engineering Journal, 2017, 326: 765-773.
����[21] Yadavali S, Jeong H H, Lee D, et al. Silicon and glass very large scale microfluidic droplet integration for terascale generation of polymer microparticles[J]. Nature Communications, 2018, 9(1): 1222.
����[22] Cui Y J, Li Y K, Wang K, et al. High-throughput preparation of uniform tiny droplets in multiple capillaries embedded stepwise microchannels[J]. Journal of Flow Chemistry, 2020, 10(1): 271-282.
����[23] Zhang J, Xu W H, Xu F Y, et al. Microfluidic droplet formation in co-flow devices fabricated by micro 3D printing[J]. Journal of Food Engineering, 2021, 290: 110212.
����[24] Jeong H H, Chen Z, Yadavali S, et al. Large-scale production of compound bubbles using parallelized microfluidics for efficient extraction of metal ions[J]. Lab on a Chip, 2019, 19(4): 665-673.
����[25] Ribeiro de Souza L, Al-Tabbaa A. High throughput production of microcapsules using microfluidics for self-healing of cementitious materials[J]. Lab on a Chip, 2021, 21(23): 4652-4659.
����[26] Kim J H, Ryu C H, Chon C H, et al. Three months extended-release microspheres prepared by multi-microchannel microfluidics in beagle dog models[J]. International Journal of Pharmaceutics, 2021, 608: 121039.
����[27] Deng C F, Yang S H, Xie R, et al. Flexible fractal integration of microfluidic modules for controllable mass production of monodisperse microdroplets[J]. Industrial & Engineering Chemistry Research, 2023, 62(32): 12690-12702.
����[28] ʯ��, ��Ф��, ������, ��. һ�����Ʊ����������ͺ����Ҽ���ɿ��ͷ�[J]. ����ѧ��, 2021, 72(1): 619-627.
����[29] ��С��, ���ص�, ʯ��, ��. һ������ͨ���ɿ��Ʊ���������ˮ/ˮ�Ҽ�����Ӧ�ͷ�[J]. �ߵ�ѧУ��ѧѧ��, 2022, 43(12): 335-344.
����[30] ������, �휏, ������. ��ͨ����������оƬ��Ƽ��Ʊ�ֲ����˾����ҵ��о�[J]. ʳƷ�뷢��ҵ, 2023, 49(3): 125-130.
����[31] Nawar S, Stolaroff J K, Ye C W, et al. Parallelizable microfluidic dropmakers with multilayer geometry for the generation of double emulsions[J]. Lab on a Chip, 2020, 20(1): 147-154.
����[32] Senn S M, Poulikakos D. Tree network channels as fluid distributors constructing double-staircase polymer electrolyte fuel cells[J]. Journal of Applied Physics, 2004, 96(1): 842-852.
����[33] Wang Y, Zhou X Y, Yang Z H, et al. An integrated and multifunctional droplet-based microfluidic platform for digital DNA amplification[J]. Biosensors and Bioelectronics, 2024, 246: 115831.
����[34] Nisisako T, Torii T. Microfluidic large-scale integration on a chip for mass production of monodisperse droplets and particles[J]. Lab on a Chip, 2008, 8(2): 287-293.
����[35] Nisisako T, Ando T, Hatsuzawa T. High-volume production of single and compound emulsions in a microfluidic parallelization arrangement coupled with coaxial annular world-to-chip interfaces[J]. Lab on a Chip, 2012, 12(18): 3426-3435.
����[36] Anshori I, Sarwono F Z, Fa'iq M A, et al. From design to performance: 3-D printing-enabled optimization of low-cost droplet microfluidics[J]. IEEE Sensors Journal, 2024, 24(1): 63-70.
����[37] Utada A S, Fernandez-Nieves A, Gordillo J M, et al. Absolute instability of a liquid jet in a coflowing stream[J]. Physical Review Letters, 2008, 100(1): 014502.
����[38] Wang Z B, Chen Z Z, Wen Y F, et al. Highly efficient droplet generation device based on a three-dimensional fractal structure[J]. Chemical Engineering Science, 2023, 282: 119227.




